Научно-производственный рецензируемый журнал «Разработка и регистрация лекарственных средств» - актуальное бесплатное прикладное издание и информационный портал для специалистов, задействованных в сфере обращения лекарственных средств. Журнал предназначен для фармацевтических предприятий-производителей и их сотрудников из отделов разработки, контроля качества, регистрации, производства и развития; сотрудников лабораторных центров, контрактно-исследовательских организаций, научных и образовательных учреждений. Включен в Перечень рецензируемых научных изданий, в которых должны быть опубликованы основные научные результаты диссертаций на соискание ученой степени кандидата наук, на соискание ученой степени доктора наук с 2015 года.
Содержание научных работ, публикуемых в журнале, соответствуют отраслям науки: фармакология, клиническая фармакология (медицинские науки); промышленная фармация и технология получения лекарств (фармацевтические науки); фармацевтическая химия, фармакогнозия (фармацевтические).
Включен в Перечень научных изданий, в которых должны быть опубликованы основные результаты исследований в рамках диссертаций по фармацевтическим наукам, представляемых к защите в диссертационных советах РУДН (от 01.10.2018 г.)
Основные пять тематических разделов журнала «Разработка и регистрация лекарственных средств» включают цикл развития лекарственного средства от его создания до получения регистрационного удостоверения. Первый раздел посвящен поиску и разработке новых лекарственных средств, второй - фармацевтической технологии и рассматривает научные и практические направления от разработки и производства исходных фармацевтических ингредиентов, технологий и оборудования – до создания стандартных и терапевтически эффективных лекарственных препаратов. Третий раздел описывает аналитические методики контроля качества; четвертый раздел посвящен подходам к оценке эффективности и безопасности лекарственных средств, проведению долклинических и клинических исследований; в пятом разделе рассматриваются вопросы валидации методик, подготовки регистрационного досье, жизненный цикл лекарственного препарата в GxP окружении.
Текущий выпуск
ОТ РЕДАКЦИИ 
Представляем вашему вниманию новое интервью в рамках цикла «Мнение лидеров». Первым гостем цикла стал генеральный директор ООО «ЦФА», главный редактор журнала «Разработка и регистрация лекарственных средств» доктор фармацевтических наук Шохин Игорь Евгеньевич.
Группа компаний Лабконцепт – официальный дистрибьютор ведущих производителей аналитического и общелабораторного оборудования. Лабконцепт предлагает комплексные решения для оснащения лабораторий разных направленностей, в том числе и для фармацевтической отрасли. Фармацевтическая отрасль России продолжает развиваться и расширять перечень и объемы выпускаемых лекарственных средств, что неминуемо влечет за собой необходимость создания новых и расширения существующих лабораторий по контролю качества выпускаемых препаратов. В условиях санкционного давления многие привычные производители аналитического оборудования ушли с рынка. При этом, растет потребность в надёжном и эффективном аналитическом и испытательном оборудовании. Группа компаний Лабконцепт предлагает решения, на практике апробированные в собственной лаборатории, в частности, тестеры растворения от Haosoo Instruments (Hanon Group) и анализаторы общего органического углерода под собственной ОЕM-маркой SILab. Обе линейки приборов соответствуют требованиям фармакопеи США, европейской фармакопеи EP и Государственной Фармакопеи РФ.
ПОИСК И РАЗРАБОТКА НОВЫХ ЛЕКАРСТВЕННЫХ СРЕДСТВ 
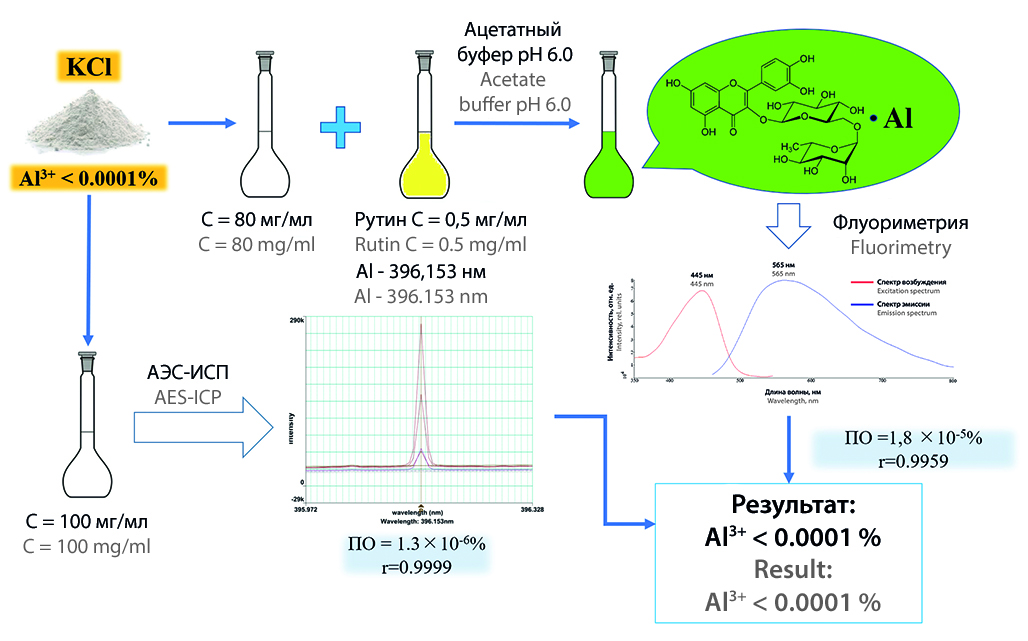
Введение. Оценка содержания примесей является важнейшим этапом в подтверждении безопасности и эффективности при контроле качества лекарственного средства. Алюминий, являясь допустимой примесью в ряде фармацевтических субстанций, способен пагубно воздействовать на организм человека, вследствие чего его содержание нормируется. Примесь алюминия в Государственной фармакопее РФ XV определяется спектрофлуориметрическим методом с применением лиганда – 8-гидроксихинолина в хлороформе. В настоящей работе предлагается заменить 8-гидроксихинолин на более доступный рутин, который также образует с металлами флуоресцирующие комплексы. Данный подход предполагает исключение из пробоподготовки этапа экстракции комплекса алюминия в хлороформ, что способствует повышению точности методики, а замена хлороформа положительным образом сказывается на безопасности.
Цель. Создание альтернативного метода спектрофлуориметрического определения примеси алюминия с помощью рутина на примере субстанции калия хлорид.
Материалы и методы. В качестве материалов исследования использовали следующие субстанции и реактивы: ГСО алюминий-иона, 1 мг/мл (ООО «ЭКРОСХИМ», Россия); ГСО железо-иона (II), 1 мг/мл (ООО «ЭКРОСХИМ», Россия); ГСО цинк-иона, 1 мг/мл (ООО «ЭКРОСХИМ», Россия); ГСО свинец-иона, 1 мг/мл (ООО «ЭКРОСХИМ», Россия); ГСО никель-иона, 1 мг/мл (ООО «ЭКРОСХИМ», Россия); ГСО медь-иона, 1 мг/мл (ООО «ЭКРОСХИМ», Россия); стандарт катиона хрома (III), 1 мг/мл (имп., Sigma-Aldrich, США); рутин (имп., Sichuan Guangsong Pharmaceutical Co., Ltd., Китай); аммоний уксуснокислый (имп., Molekula GmbH, Германия), уксусная кислота ледяная (х. ч., АО «База № 1 Химреактивов», Россия); калия хлорид (ФС, ООО «МЗХР», Россия). Спектрофлуориметрическое исследование проводилось на приборе FL 6500 (PerkinElmer Inc., США). Содержание примеси алюминия также оценивалось с использованием атомно-эмиссионного спектрометра с индуктивно связанной плазмой (АЭС-ИСП) Optima 8000 (PerkinElmer Inc., США) и стандартного образца Multi-Element Solution (PerkinElmer Inc., США).
Результаты и обсуждение. Подход, приведенный в статье, исключает использование 8-гидроксихинолина в хлороформе и заменяет его на рутин в 70%-м спирте этиловом. Комплекс алюминия с рутином имеет длину волны возбуждения при 445 нм и длину волны эмиссии при 565 нм. Предложенная методика была апробирована на субстанции калия хлорид для оценки показателя «Алюминий», содержание которого не должно превышать 0,0001 %. Валидация методики осуществлялась по трем параметрам: «специфичность», «линейность» и «предел обнаружения» (ОФС.1.1.0012). Сопоставление полученных данных проводилось с применением атомно-эмиссионной спектроскопии, в ходе которой была доказана релевантность методики.
Заключение. Разработан эргономичный способ спектрофлуориметрического определения примеси алюминия с помощью рутина с апробацией на субстанции калия хлорид. Результаты, полученные в ходе эксперимента, были подтверждены методом АЭС-ИСП.
Введение. Поиск новых методов терапии немелкоклеточного рака легкого (НМРЛ) является актуальной задачей современной науки. Гефитиниб – таргетный препарат, широко применяемый при терапии НМРЛ у пациентов с мутацией в домене тирозинкиназы рецепторов эпидермального фактора роста. Однако применение гефитиниба и других препаратов из группы ингибиторов тирозинкиназы ограничено быстроразвивающейся резистентностью, поэтому исследования, направленные на поиск путей преодоления лекарственной устойчивости, представляют огромный интерес.
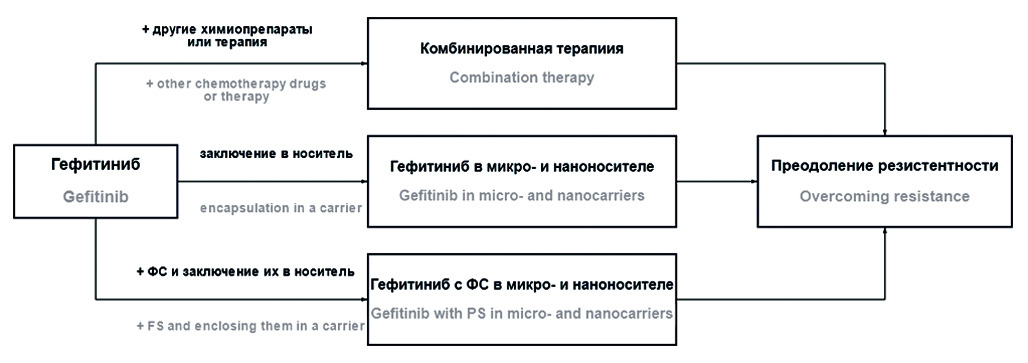
Текст. Обзор посвящен применению гефитиниба в современных разработках: введению в различные системы направленной доставки (липосомы, мицеллы, микросферы и др.), изучению его в комбинации с другими химиотерапевтическими агентами, а также в комбинации с фото- или термочувствительными соединениями в составе различных микро- и наноструктурированных комплексов.
Заключение. В результате проведенного анализа литературных данных показано, что, несмотря на то, что гефитиниб является препаратом первого поколения, зарубежные и российские исследователи считают его достаточно перспективным для дальнейшего применения при терапии НМРЛ. При этом разработки ведутся как в области расширения комбинированной терапии, так и в области создания комплексных структур направленного действия, в которые, кроме гефитиниба, введены фотосенсибилизаторы или другие соединения, обладающие фото- или термочувствительными эффектами.
ФАРМАЦЕВТИЧЕСКАЯ ТЕХНОЛОГИЯ 
Введение. В современной медицине ужесточаются требования к качеству используемых материалов, серьезное беспокойство вызывает проблема бактериальной и грибковой контаминации, возникающая при использовании полимерных изделий на основе силиконов, находящихся в тесном контакте с тканями и биологическими жидкостями организма. В связи с этим представляется актуальным введение в силиконовые изделия медицинского назначения различных биологически активных веществ (БАВ), в том числе с антимикробными свойствами.
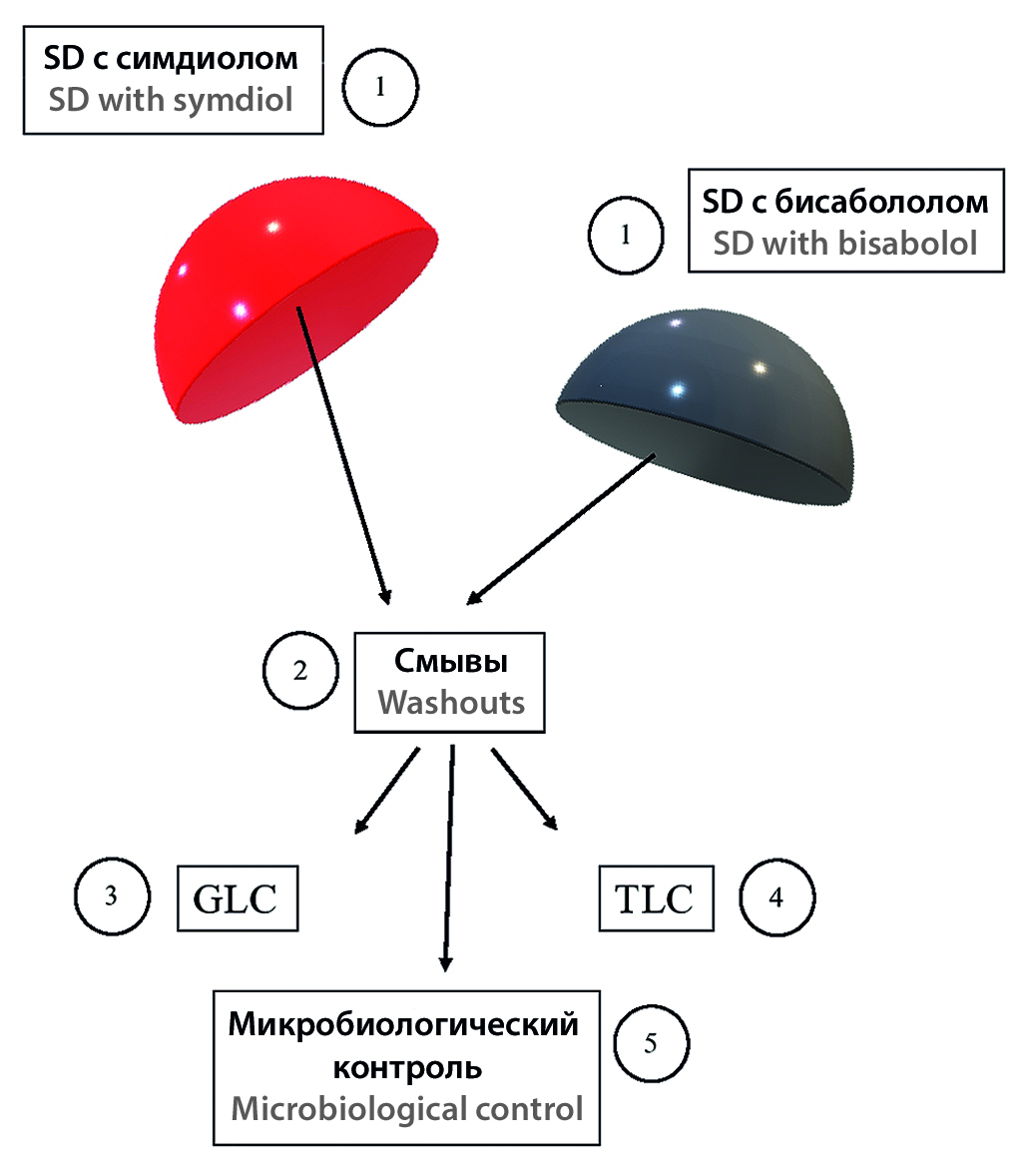
Цель. В работе была изучена целесообразность введения БАВ в силиконовые изделия медицинского назначения для улучшения их качества и предотвращения негативных последствий их использования. Авторы статьи ставили перед собой задачу доказать возможность высвобождения выбранных БАВ из силиконовых изделий в процессе контакта с кожей и, как следствие, возникающий в ходе высвобождения БАВ бактериостатический эффект. Для этого важно было подтвердить факт присутствия БАВ в смывах с силиконовых дисков, что, в свою очередь, является доказательством того, что биологически активные добавки, первоначально равномерно распределенные в объеме силиконового диска, способны диффундировать к поверхности и далее высвобождаться с нее при механическом воздействии, а также при обработке спиртом и спиртосодержащими растворами.
Материалы и методы. В качестве БАВ выбраны симдиол и бисаболол – вещества с доказанными антимикробными, противовоспалительными и увлажняющими свойствами. Использовали бисаболол в виде препарата «Драгосантол 100» и симдиол в виде «SymDiol 68Т». В качестве имитационной модели силиконовых лайнеров использовали силиконовые диски (СД), импрегнированные БАВ (0,2 % от объема). Высвобождение БАВ из имитационных моделей силиконовых лайнеров контролировали методами тонкослойной и газожидкостной хроматографии.
Результаты и обсуждение. Была отработана методика введения БАВ в СД, подобраны оптимальные концентрации этих веществ для введения в силиконовую основу. Подтверждена возможность высвобождения импрегнированных добавок из изделия. Полученные в ходе эксперимента данные позволяют с уверенностью утверждать, что из силиконового диска даже при кратковременном и малоинтенсивном механическом контакте с кожей происходит высвобождение введенного препарата (симдиола и бисаболола), обладающего стабильным бактериостатическим действием на широкий спектр микроорганизмов. Процессу высвобождения БАВ из СД также способствует периодическая обработка изделия спиртосодержащими растворами, необходимость которой предусмотрена правилами эксплуатации. Полученные результаты хроматографических исследований вполне коррелируют с данными предшествующих микробиологических опытов по изучаемой проблеме. Высвобождение изученных БАВ из полимерных изделий в процессе эксплуатации в течение не менее 3 месяцев подтверждает целесообразность введения БАВ в силиконовую основу.
Заключение. В исследовании было подтверждено высвобождение биологически активных добавок из силиконовых изделий, применяемых в ортопедии. Введение БАВ в имитационные модели силиконовых лайнеров, безусловно, улучшает качество этих продуктов медицинского назначения и делает целесообразным их применение в различных областях протезирования и ортезирования.
Введение. Медицинские глины представлены полиминеральными сорбентами с преобладанием основополагающего глинистого минерала, от концентрации которого зависит качество минерального сырья и его адсорбционная активность. Одним из методов повышения качества минерального сырья является его активация при помощи ультразвуковой обработки.
Цель. Изучение влияния ультразвука на активацию и адсорбционную активность минеральных сорбентов.
Материалы и методы. В качестве объектов исследования использовали клиноптилолитовое минеральное сырье Холинского месторождения (Забайкальский край), монтмориллонитовое минеральное сырье Белгородского месторождения (Белгородская область) и каолинитовое минеральное сырье Еленинского месторождения (Челябинская область). Для ультразвуковой обработки использовали высокочастотную установку УЗДН-1. Определение адсорбционной активности проводили по метиленовому синему.
Результаты и обсуждение. Исследовано влияние ультразвука на активацию минеральных сорбентов при частоте ультразвуковой волны 40 кГц в течение пяти минут. Установлено, что среднее содержание клиноптилолита с учетом всех фракций в глине Холинского месторождения увеличивается на 20 %, среднее содержание монтмориллонита с учетом всех фракций в глине Белгородского месторождения увеличивается на 14 %, среднее содержание каолинита с учетом всех фракций в глине Еленинского месторождения увеличивается на 18 %. Исследовано влияние ультразвука на адсорбционную активность минеральных сорбентов. Использование ультразвуковой обработки повышает адсорбционную активность минеральных сорбентов на 12–19 %.
Заключение. Разработанную методику активации минеральных сорбентов посредством ультразвуковой обработки возможно применять для активации минеральных сорбентов путем повышения концентрации основополагающего минерала (клиноптилолита, монтмориллонита, каолинита), а также увеличения их адсорбционной активности.
Введение. На сегодняшний день блок-сополимеры ПЭО и ППО (полоксамеры, плюроники, проксанолы) являются одними из наиболее востребованных фармацевтической и биотехнологической промышленностью полимеров. Они находят свое применение в качестве эффективных неионогенных поверхностно-активных веществ, стабилизаторов биологических мембран, элементов систем направленной доставки, солюбилизаторов, а также в качестве вспомогательных веществ в технологии традиционных лекарственных форм – гелеобразователей, лубрикантов и т. д. На протяжении последних пятидесяти лет крупнейшим мировым производителем полоксамеров являлся немецкий химический концерн BASF. Однако на сегодняшний день в Российской Федерации существует риск дефектуры, что обозначает актуальность импортозамещения данного эксципиента.
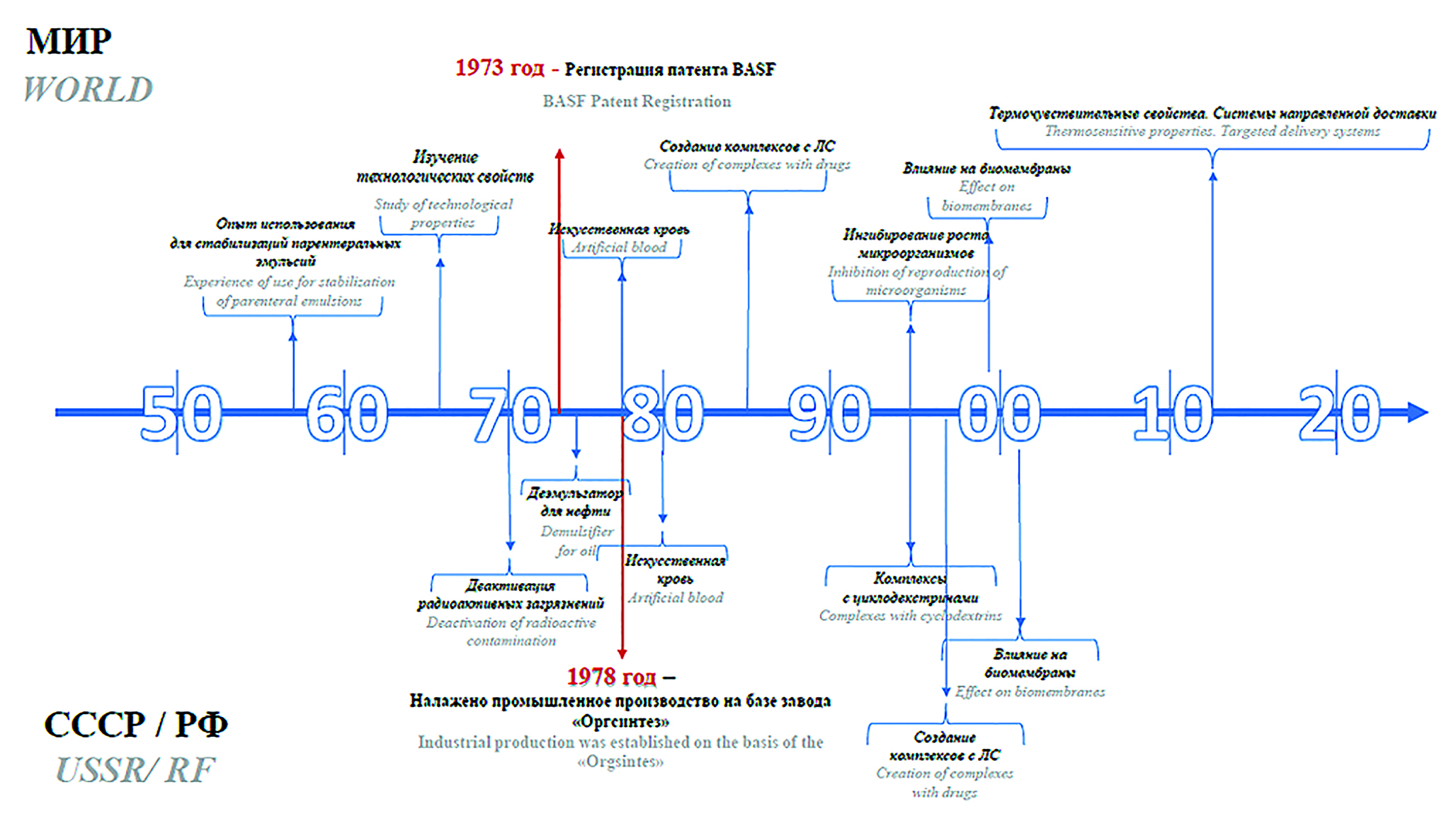
Текст. Целью настоящего обзора являлось освещение опыта производства и внедрения блок-сополимеров ПЭО и ППО в новые разработки советскими и российскими учеными, сравнение их с опытом иностранных исследовательских групп, необходимое для оценки потенциала к импортозамещению. Блок-сополимеры ПЭО и ППО были известны в Советском Союзе с конца 1960-х годов – они упоминаются в учебных пособиях 1964 и 1973 годов. Отечественные блок-сополимеры ПЭО и ППО находили применение в нефтеперерабатывающей промышленности, в некоторых отраслях легкой промышленности, а также при дезактивации радиоактивных отходов. Собственный синтез блок-сополимеров ПЭО и ППО был налажен в 1978 году на базе завода «Оргсинтез». Советские полоксамеры выпускались под маркой «проксанол» в широком ассортименте соотношений звеньев ЭО и ПО и молекулярных масс. Необходимо отметить, что на сегодняшний день в Российской Федерации по-прежнему выпускают промышленные партии солюбилизатора эмуксол-268, являющегося близким по своим свойствам к известному полоксамеру 188, а также проводится синтез под заказ блок-сополимеров с другими соотношениями звеньев ЭО и ПО.
Заключение. Как показал ретроспективный анализ, у современной российской промышленности достаточно опыта и ресурсов для налаживания синтеза блок-сополимеров ПЭО и ППО, необходимых для производства лекарственных препаратов и разработки инновационных систем доставки лекарств. По материалам проведенного систематического обзора был впервые составлен наиболее полный реестр известных марок блок-сополимеров ПЭО и ППО, синтезированных за последние 50 лет в нашей стране и за рубежом, с подробной характеристикой их физико-химических свойств.
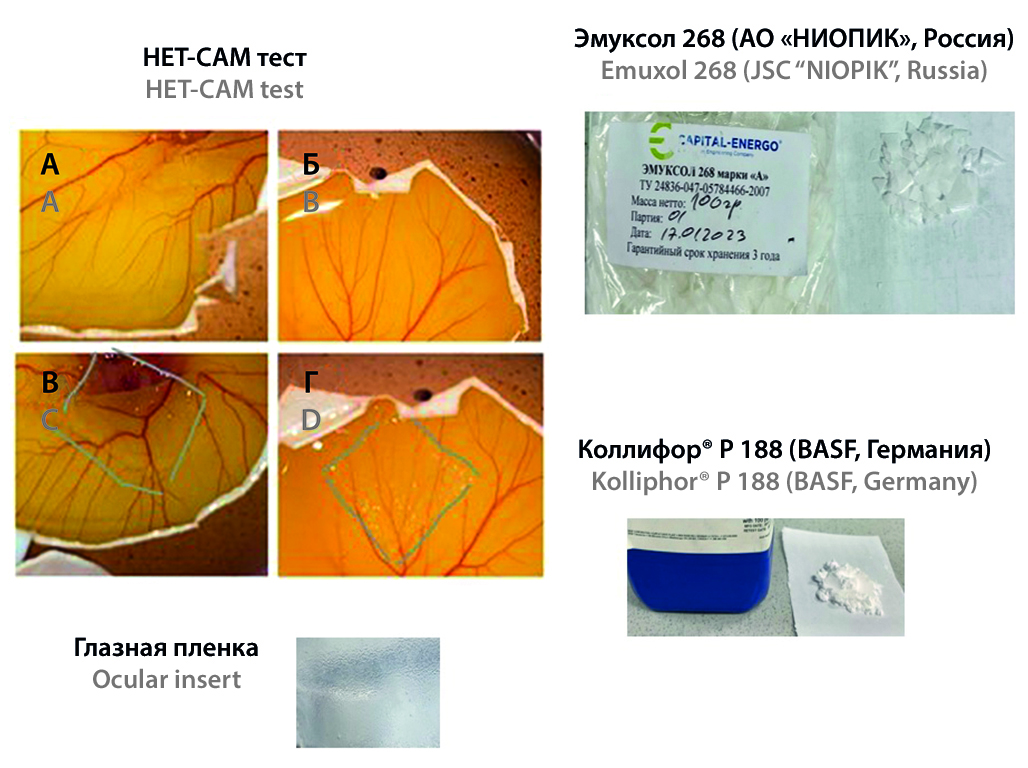
Введение. Эмуксол-268 (АО «НИОПИК», Россия) является отечественным блок-сополимером, по физико-химическим и биологическим свойствам близким к полоксамеру Kolliphor® P 188 (Pluronic F68) производства компании BASF. Однако сравнение технологических свойств данных полимеров для оценки перспектив введения их в лекарственные формы до этого не проводилось.
Цель. Целью исследования было на примере разработки глазной лекарственной пленки продемонстрировать взаимозаменяемость вспомогательных компонентов путем сравнения результатов тестирования лекарственной формы по таким параметрам качества, как эластичность, толщина, мукоадгезия, рH, время биодеградации, тест на определение раздражимости (тест хориоаллантоисной мембраны куриного яйца, HET-CAM-тест).
Материалы и методы. В эксперименте использовали полоксамеры эмуксол-268 (АО «НИОПИК», Россия) и Kolliphor® P 188 (BASF, Германия), гидроксиэтилцеллюлозу (Natrosol™ 250 HHX, Ashland Global Holdings Inc., США) и глицерин (ООО «Тульская фармфабрика», Россия). В качестве скрининговых методов для выявления примуществ композиции использовали тестирование по таким показателям, как эластичность, толщина, мукоадгезия, рH, время биодеградации, раздражимость (HET-CAM-тест).
Результаты и обсуждение. Результаты эксперимента доказали, что использование отечественного аналога позволяет создать глазную пленку с улучшенными параметрами качества. Разница показателя эластичности пленок отличается в 1,3 раза, мукоадгезии – в 1,7 раза, времени биодеградации – в 2,5 раза, в связи с чем можно предположить, что пленка на основе отечественного полимера в большей мере способствует увеличению времени контакта с поверхностью глаза, тем самым обеспечивая длительный контакт лекарственной формы и улучшение ее биодоступности. Полученные результаты могут быть обусловлены разницей средней молекулярной массы гидрофобной полиоксипропиленовой части, которая для эмуксола-268 составляет 2600 Да, а для Kolliphor P188 – 1800 Да. Метод HET-CAM продемонстрировал одинаковые результаты для двух композиций, оба состава не обладают раздражающим эффектом.
Заключение. Подводя итоги, можно сделать вывод, что доступный на российском фармацевтическом рынке единственный аналог Kolliphor® P188 эмуксол-268 компании АО «НИОПИК» является перспективным веществом для замены в разработке офтальмологических лекарственных форм. Несмотря на отличия отечественного блок-сополимера по физико-химическим свойствам от заменяемого полоксамера 188, его введение в состав плацебо-пленок давало улучшенные результаты по показателям качества, что было выявлено в ходе биофармацевтического анализа.
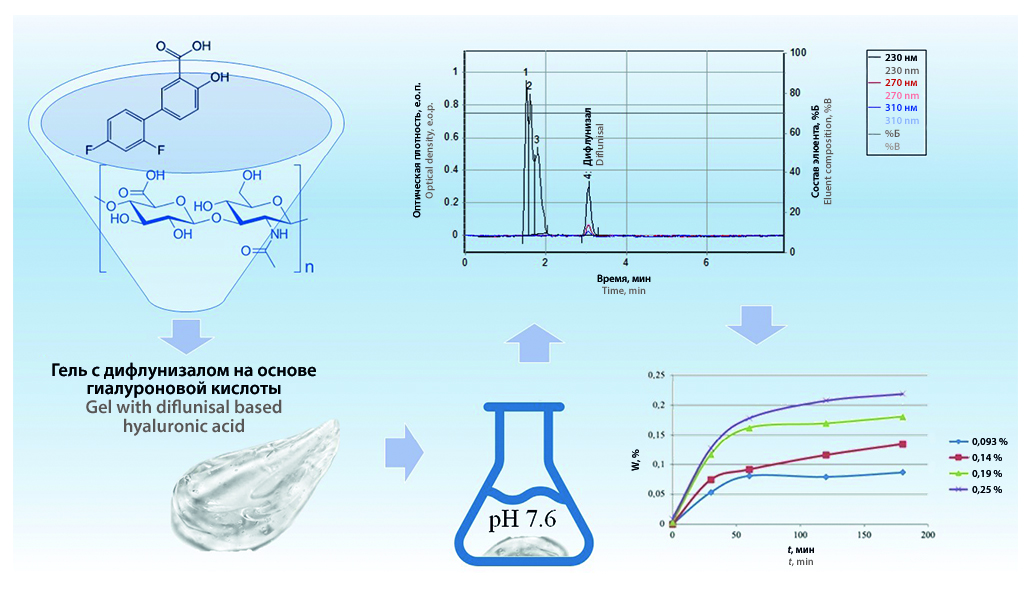
Введение. Клинически доказана эффективность дифлунизала при лечении амилоидоза сердца. В настоящее время в мире зарегистрированы только таблетированные формы дифлунизала, однако длительное применение НПВП приводит к характерным побочным эффектам. Поэтому сейчас активно разрабатываются системы доставки дифлунизала (в том числе формы для наружного применения), позволяющие уменьшить побочные эффекты, улучшить его биодоступность.
Цель. Изучение динамики высвобождения действующего вещества дифлунизала из полимерной матрицы гиалуроновой кислоты.
Материалы и методы. Объектами исследования являются гели дифлунизала в гиалуроновой кислоте с концентрацией основного вещества 0,093, 0,14, 0,19 и 0,25 %. Количественное определение проводили методом обращенно-фазовой ВЭЖХ с использованием хроматографической колонки Prontosil С18,120-5, 75 × 2 мм, термостатируемой при 40 °С. Элюент: фосфатный буферный раствор с рН 3,0 и ацетонитрил (30 : 70), скорость потока 0,1 мл/мин. Детектировали элюаты на длинах волн 230, 270, 310 нм.
Результаты и обсуждение. Разработана методика определения дифлунизала в матрице гиалуроновой кислоты методом ВЭЖХ. Высвобождение действующего вещества из матриц проводили в среде фосфатного буферного раствора с рН 7,6. Исследуемая система доставки значительно увеличивает растворимость дифлунизала в водном растворе по сравнению с растворением субстанции. Степень высвобождения для всех образцов превышает 90 % через 3 часа после начала эксперимента, при этом большая часть действующего вещества высвобождается в течение часа.
Заключение. Полученные данные позволяют утверждать, что профиль высвобождения характерен для биодеградируемых матриц и диффузионно-контролируемых систем доставки. Достигнута полнота извлечения дифлунизала из ГК при использовании в качестве среды растворения ФБР с рН 7,6.
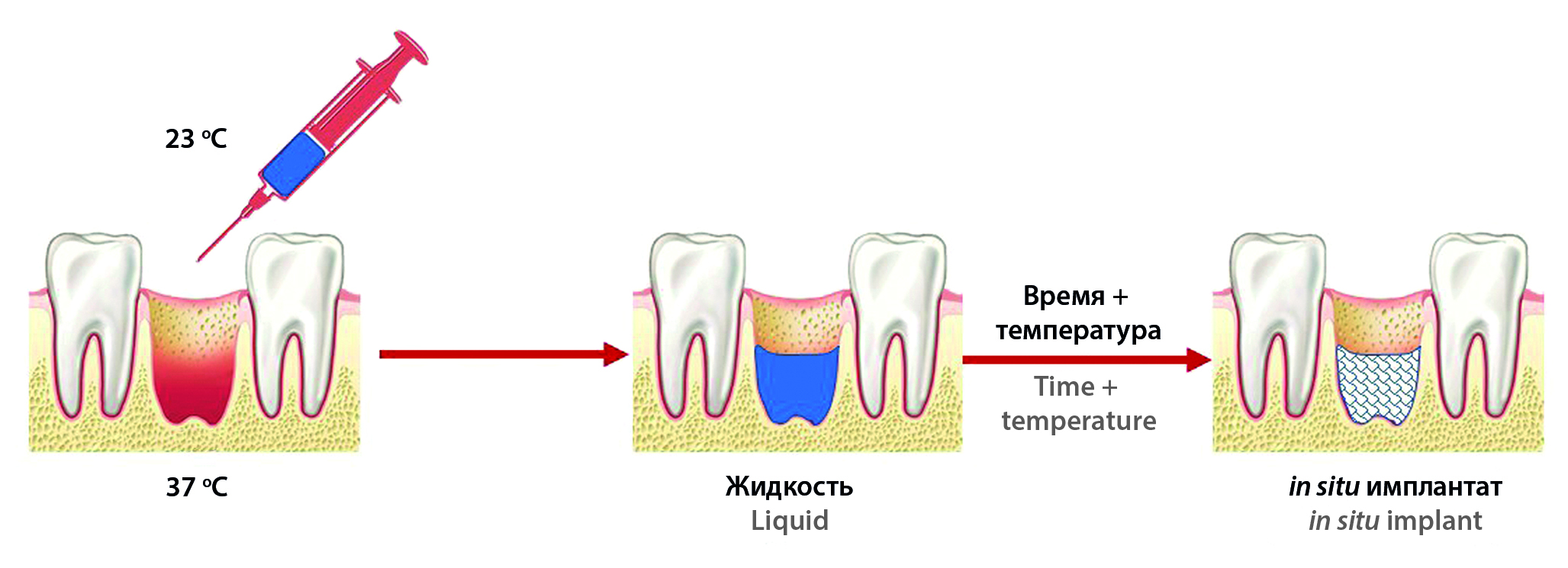
Введение. Проблема обезболивания после хирургического вмешательства актуальна в современной стоматологии, так как контроль над болью является важной частью лечения. Помимо обезболивания, существуют и другие проблемы пострезекционной терапии – кровотечение из раны, воспалительный процесс. Современная стоматологическая практика не располагает системой направленной доставки или медицинским изделием анальгезирующего, противовоспалительного, анестезирующего или кровоостанавливающего действия, обеспечивающими высокую приверженность пациентов проводимой пострезекционной терапии.
Текст. Для решения данной проблемы может быть предложена разработка системы in situ, а именно имплантата – лекарственной формы, формирующейся непосредственно в месте введения, в альвеолярной лунке. Такая система направленной доставки обладает сразу несколькими преимуществами, к которым можно отнести: отсутствие необходимости в применении перевязочного медицинского материала; отсутствие риска вторичной контаминации; точность дозирования и таргетность доставки в локус поражения; высокую мукоадгезию системы к месту нанесения; длительность высвобождения активного ингредиента и другие. Целью обзора является обоснование возможности и актуальности разработки новой системы в форме in situ имплантата для применения в стоматологической пострезекционной практике. Исследование проводилось по основным базам публикаций (Scopus, Web of Science, PubMed и другие), а также в базе данных патентного поиска по материалам, опубликованным за период с 2000 года по настоящее время. В ходе исследования были описаны существующие на данный момент in situ системы для решения стоматологических проблем, которые могли бы служить прототипом систем для доставки обезболивающего вещества непосредственно в лунку зуба; полимеры, использующиеся для их создания и возможности высвобождения лекарственных веществ; а также приводится характеристика существующих лекарственных форм, применяющихся как местно, так и для оказания системного действия с целью обезболивания, в сравнении с системами in situ, которые имеют определенные достоинства и большой потенциал для развития.
Заключение. По результатам работы сделано заключение о возможности проведения фармацевтической разработки имплантатов in situ для стоматологического применения, а также выделены наиболее перспективные полимеры для осуществления фазового перехода в альвеолярной лунке.
МЕТОДЫ АНАЛИЗА ЛЕКАРСТВЕННЫХ СРЕДСТВ 
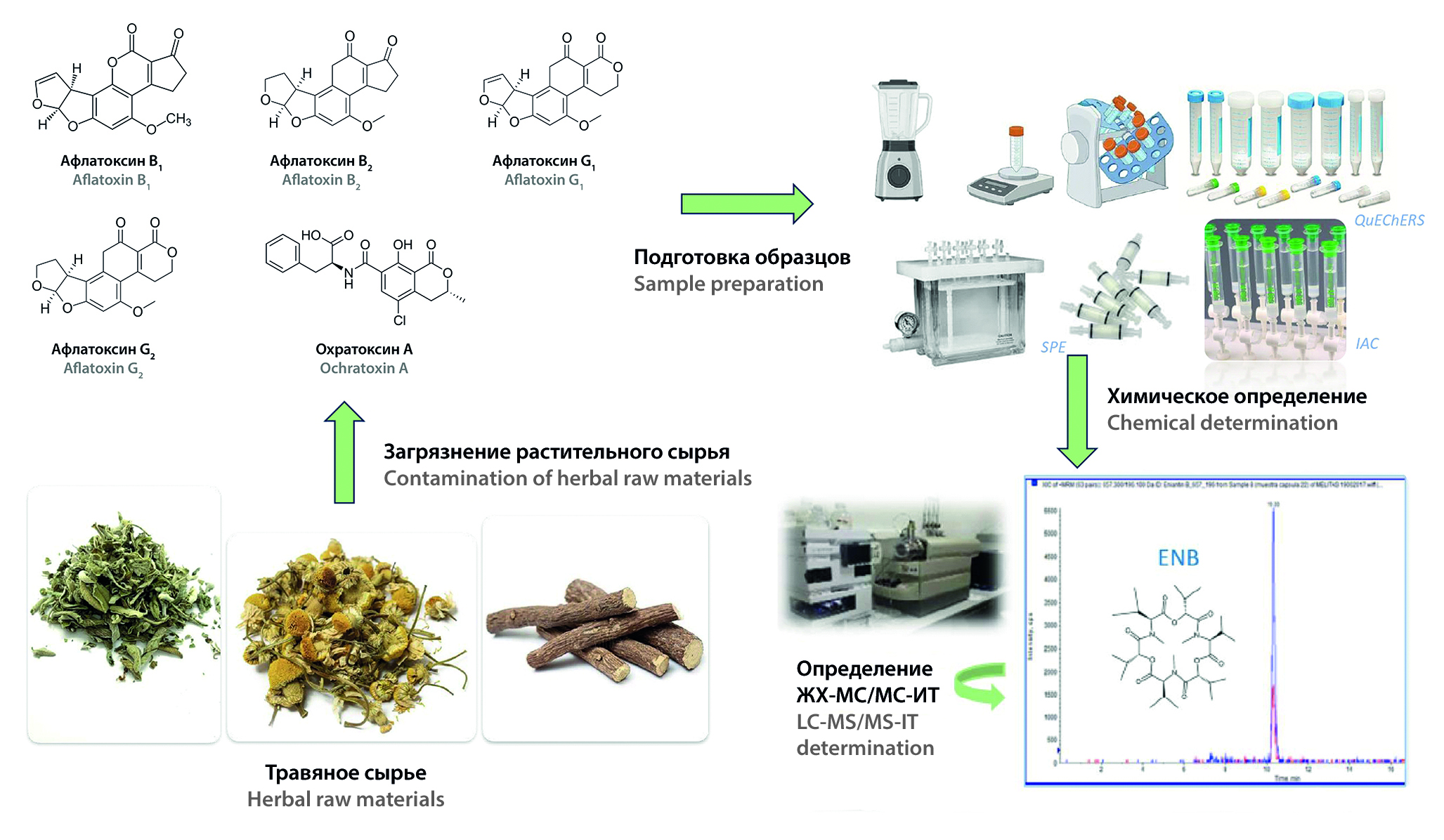
Введение. Афлатоксины и охратоксин А представляют собой вторичные метаболиты микроскопических плесневых грибов и несут серьезную угрозу здоровью человека и животных. Данные токсины являются канцерогенными, тератогенными, гепатотоксичными, нефротоксичными веществами, также классифицированы Международным агентством по изучению рака (IARC) как канцерогены IA и IIB класса. В настоящее время предельно допустимые концентрации афлатоксинов и охратоксина А в Российской Федерации регулируются только в продуктах питания на основании технического регламента Таможенного союза 021 «О безопасности пищевой продукции», лекарственное растительное сырье не регламентируется. Неблагоприятные экологические и биологические условия (температура, влажность, качество воздуха, насекомые и т. д.) на этапах послеуборочной обработки и хранения могут способствовать заражению плесневыми грибами, что может привести к контаминации лекарственного сырья афлатоксинами и охратоксином А. В связи с этим важным этапом контроля качества сырья является изучение методов анализа, которые используются в современной аналитической практике, и выбор чувствительного метода для обнаружения данных токсинов.
Текст. В данном обзоре были рассмотрены существующие методы очистки проб, использующиеся на этапе пробоподготовки: твердофазная экстракция, иммуноаффинная колонка, QuEChERS. Были изучены все современные методы анализа для идентификации афлатоксинов и охратоксина А в лекарственном растительном сырье: тонкослойная хроматография, жидкостная хроматография, газовая хроматография и скрининговые методы.
Заключение. В качестве наиболее востребованного метода при подготовке проб к анализу был выделен метод QuEChERS, основанный на технологии экстракции твердых фаз. Этот метод сочетает в себе вариабельность подходов к очистке пробы и позволяет исследовать более широкий спектр токсинов. Метод высокоэффективной жидкостной хроматографии, обладающий высокой селективностью, многокомпонентностью анализа и низкими пределами обнаружения, был выделен как самый востребованный метод для проведения качественного и количественного анализа.
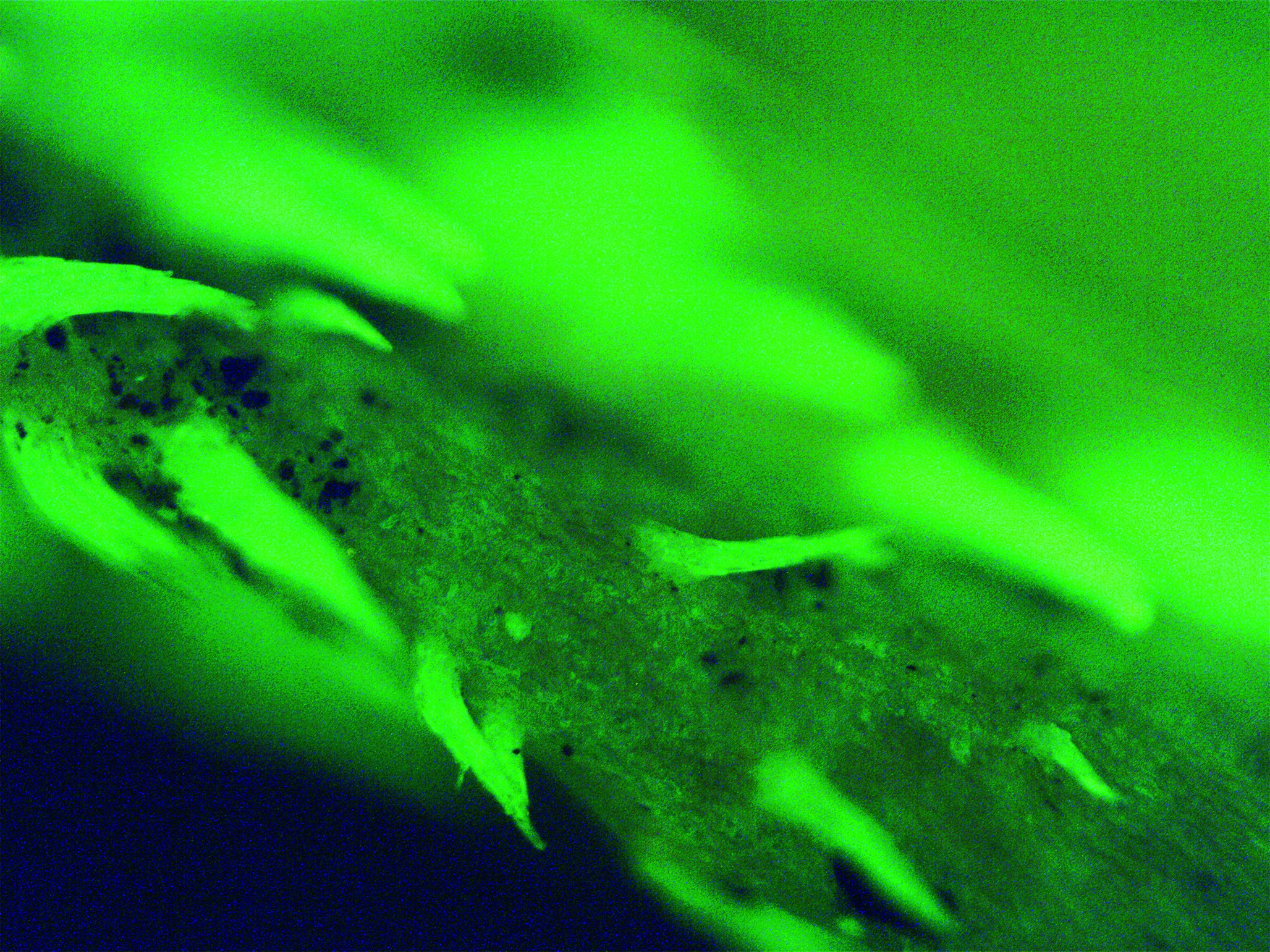
Введение. Вопрос стандартизации и оценки качества лекарственного растительного сырья в настоящее время является одним из важнейших. Для этого оценивается ряд параметров, первичным из которых является подлинность анализируемого растительного объекта. Проблема идентификации официнальных, а также новых перспективных видов растений, особенно при наличии близкородственных примесных видов, характерна для многих семейств и родов, среди которых можно выделить род Persicaria Mill. (горец). Два вида этого рода, на которые разработана нормативная документация (ФС), используются в медицинской практике. Схожесть морфолого-анатомических признаков видов растений диктует необходимость использования дополнительных современных методов анализа, позволяющих всесторонне выявлять характерные особенности видов. Одним из подобных селективных методов диагностики растительного сырья, наряду с общеизвестными и используемыми в фармацевтическом анализе, является люминесцентная микроскопия.
Цель. Целью являлось изучение особенностей люминесценции близкородственных видов рода горец Persicaria Mill. для усовершенствования процесса стандартизации официнальных видов сырья.
Материалы и методы. Для работы были использованы 10 видов рода Persicaria Mill. семейства Polygonaceae Juss., наиболее часто встречающиеся в Центральном Черноземье: P. maculosa Gray, P. tomentósa Bicknell, P. lapathifólia Delarbre, P. nodósa Opiz, P. scábra Moldenke, P. brittingeri Opiz, P. hydropiper Delarbre, P. mínor Opiz, P. amphibia Delarbre, P. amphibia var. terréstris Munshi & Javeid. Растения срезали на высоте около 15 см от почвы во время массового цветения летом 2020 года в Воронежской области, высушивали в тени. Предварительно перед проведением исследования растения были разделены на морфологические составляющие (стебли, листья, черешки, раструбы, цветки, плоды), для чего использовались гербарные образцы в высушенном виде, и рассматривались отдельные части, расправленные на предметном стекле. Для оценки люминесценции объектов использовали микроскоп «Микромед-3 Люм» (Россия) с корпусом люминесцентной насадки.
Результаты и обсуждение. Выявлено, что общим для всех изученных видов является интенсивная флуоресценция крупных трихом, проводящей системы, замыкающих клеток устьиц, утолщений клеточных стенок и – у некоторых видов – содержимого вместилищ и железок. Выявлен ряд характерных особенностей люминесценции тканей для изучаемых видов: P. hydropiper на всех морфологических частях имеет многочисленные ярко светящиеся вместилища и железки. Для P. maculosa впервые установлено наличие крупных вместилищ по жилкам. Околоцветник, железки и нитевидные волоски раструба P. brittingeri имеют отчетливо видимую желтовато-зеленую люминесценцию. Железки листа P. tomentósa, в отличие от других видов, не имеют свечения. Околоцветники P. scábra и P. tomentósa имеют желтовато-оранжевое свечение. Пленчатые трихомы хорошо заметны у P. lapathifólia и выделяются коричневатым оттенком. Наибольшее количество длинных пучковых трихом, имеющих яркое зеленоватое свечение, характерно для P. amphibia var. terréstris.
Заключение. Метод люминесцентной микроскопии был впервые применен для анализа и выявления идентификационных параметров близкородственных видов рода Persicaria, установлены и визуализированы новые диагностические особенности, способствующие максимально точной идентификации видов рода Persicaria.
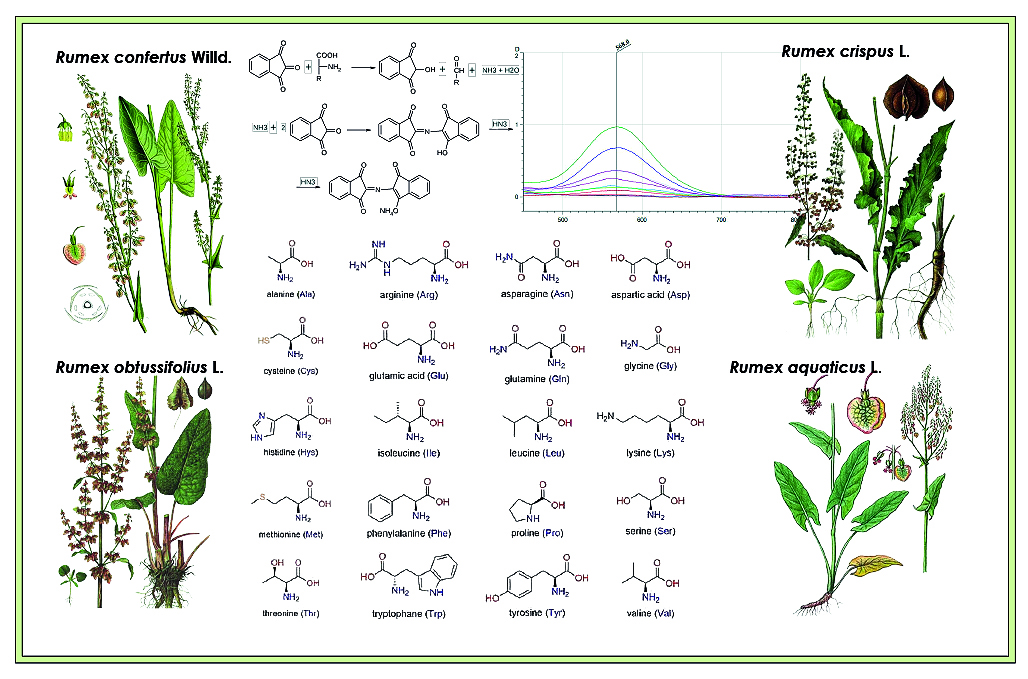
Введение. Аминокислоты (АК) являются первичными метаболитами в растениях. Одна из функций – синтез фенольных соединений. Препараты и биологически активные добавки на основе лекарственных растений могут быть доступным источником заменимых и незаменимых АК. Большое содержание АК в свободном виде в растительном сырье чаще всего указывает на наличие биотического и абиотического стресса. Помимо этого – важной задачей является определение динамики накопления биологически активных веществ в зависимости от фенологической фазы развития растения.
Цель. Сравнительное изучение качественного состава и динамики накопления АК в подземных органах четырех представителей рода Rumex: R. confertus, R. crispus L., R. obtusifolius L., R. aquaticus L. трех различных фаз вегетации.
Материалы и методы. В качестве анализируемых растворов использовались водные извлечения из подземных органов изучаемых видов рода Rumex, получаемые для качественного и количественного исследования по двум различным методикам. На хроматографические пластинки марки TLS Silica gel 60 F254 (Merk, Германия) 20 × 20 см наносили извлечения микрошприцем (ООО «Цвет», Россия). После элюирования пластинки обрабатывали 2%-м раствором нингидрина. Количественное определение проводилось на спектрофотометре СФ-2000 (ООО «ОКБ Спектр», Россия).
Результаты и обсуждение. Было проведено определение АК методом ТСХ и оценено количественное содержание методом спектрофотомерии в подземных органах четырех представителей рода Rumex: R. confertus, R. crispus L., R. obtusifolius L., R. aquaticus L. Трех различных фаз вегетации.
Заключение. Наиболее разнообразные профили АК были обнаружены в фазу отмирания надземной части у всех видов Rumex (до 9 зон адсорбции), наименее разнообразные в фазу цветения (от 2 до 4 зон адсорбции). Количественное содержание АК наименьшим было в фазе цветения, возрастало в фазу отрастания и достигало пика в фазу отмирания, исключением является R. crispus L., у которого наибольшее количественное содержание АК было отмечено в фазу отрастания.
Введение. Одним из наиболее перспективных типов иммунодатчиков являются пьезокварцевые иммуносенсоры. Единоразовое использование биосенсоров является финансово затратным, что делает регенерацию поверхности биосенсора пьезокварцевых иммуносенсоров актуальной задачей. Регенерация имеет решающее значение для поддержания работоспособности датчика и возможности повторного использования. В данной статье понятия «иммуносенсор» и «иммунобиосенсор» являются взаимозаменяемыми и используются для обозначения одного и того же типа биосенсоров, работающих на основе иммунохимических взаимодействий «антиген – антитело».
Текст. В обзоре обсуждаются особенности, принципы работы и применение пьезокварцевых иммуносенсоров QCM. Особое внимание уделяется проблеме регенерации поверхности биосенсоров как ключевому аспекту обеспечения их эффективной работы и возможности многократного использования. Рассматриваются различные методы регенерации и их преимущества. Повторная активация биослоя на электроде QCM обеспечивает его стабильность и работоспособность в течение продолжительного времени. Это особенно ценно в клинических и научных исследованиях. Возможность многократного использования биосенсора позволяет снизить затраты на материалы и сократить производство отходов, что актуально с экологической и экономической точек зрения. Также воспроизведение анализа различных аналитов на одной и той же поверхности обеспечивает гибкость в многопараметрических исследованиях. Важно подчеркнуть, что удаление остаточных анализируемых веществ и процесс регенерации биослоя способствуют надежности, селективности, повышенной чувствительности и возможности проведения воспроизводимых измерений.
Заключение. Авторами был проведен анализ научной литературы, в результате чего установлено, что регенерация биослоя имеет решающее значение для поддержания работоспособности датчика и возможности повторного использования, которую определяет сила взаимодействия «антиген – антитело», поэтому условия должны быть подобраны индивидуально для каждой пары «антиген – антитело». В обзоре подробно рассмотрены три основных подхода к регенерации пьезоэлектрических преобразователей: с использованием химического метода, кислородно-плазменного метода, при помощи раствора «пираньи».
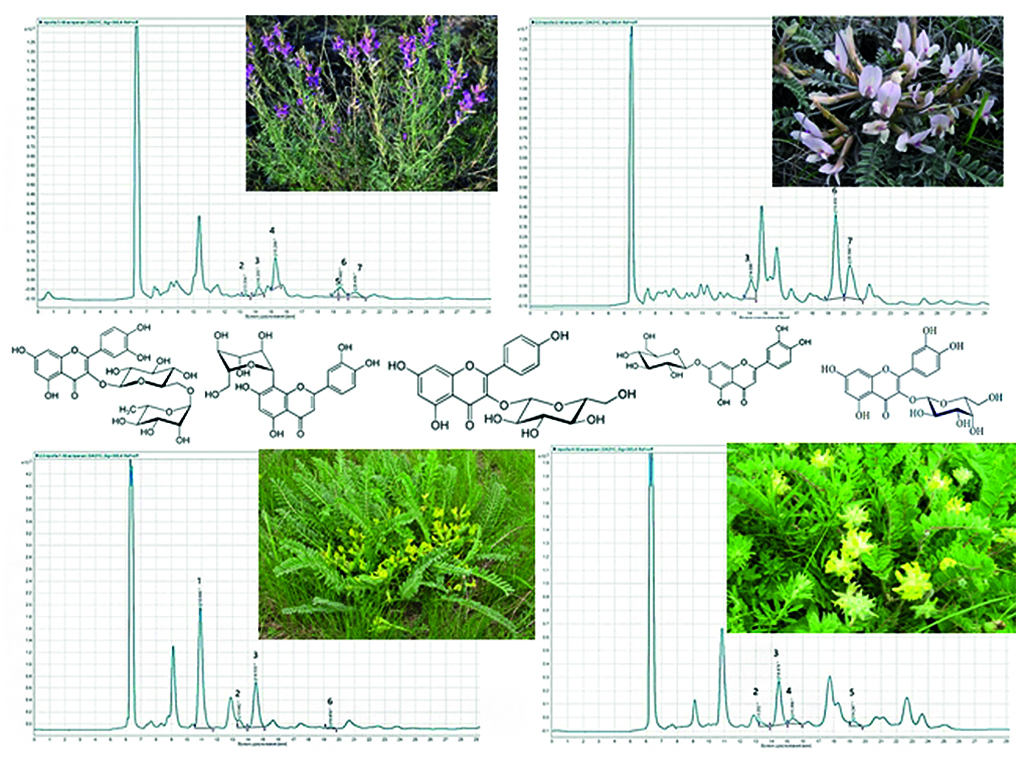
Введение. Поиск новых перспективных источников биологически активных веществ является одной из задач современной фармакогнозии. Среди огромного разнообразия видов рода Astragalus L. изучены лишь некоторые из них. Кроме этого, ни один из них не включен в актуальное издание Государственной фармакопеи РФ. На наш взгляд, интерес представляет исследование четырех видов этого рода (А. dasyanthus, А. varius, А. testiculatus, А. henningii), произрастающих на территории Поволжья.
Цель. Исследование гликозидного состава флавоноидов травы астрагалов четырех видов (А. dasyanthus, А. varius, А. testiculatus, А. henningii) методом ВЭЖХ-УФ с использованием внешних стандартов.
Материалы и методы. Материалом служили образцы травы астрагалов (А. dasyanthus, А. varius, А. testiculatus, А. henningii), заготовленные на территории Саратовской области в соответствии с основными правилами сбора и заготовки и высушенные до воздушно-сухого состояния. Анализу подвергались водно-спиртовые извлечения (1 : 50). Качественный и количественный анализ гликозидов флавоноидов проводили на хроматографе Agilent 1260 (Agilent Technologies, США), снабженном диодно-матричным детектором, ручным вводом проб (ручной инжектор Agilent G1328C, Agilent Technologies США) и системой для сбора и обработки хроматографических данных Agilent Open Lab CDS. Градиент элюирования был подобран индивидуально с использованием в качестве растворителей 0,1%-го раствора ортофосфорной кислоты / ацетонитрила. Соединения идентифицировали по временам удерживания и УФ-спектрам стандартных образцов (СО). Количественное содержание каждого обнаруженного компонента выражали в мг/г сухого сырья. Все исследования были повторены пятикратно, результаты статистически обработаны с помощью MS Excel 2010.
Результаты и обсуждение. Исследованы хроматографические профили водно-спиртовых извлечений из травы четырех видов астрагалов. Обнаружены отличия как в качественном составе, так и в количественном содержании флавоноидных гликозидов в траве анализируемых видов. Наибольшее число соединений обнаружено в траве А. varius (6 соединений), в траве А. dasyanthus и А. henningii идентифицировано 4 соединения, а в траве А. testiculatus – 3 соединения. Доминирующими компонентами в траве А. henningii являются ориентин и рутин, в траве А. testiculatus и А. varius – цинарозид, а у А. dasyanthus – рутин.
Заключение. Была разработана методика ВЭЖХ-УФ-определения количественного содержания флавоноидных гликозидов в извлечениях из травы четырех видов астрагалов (А. dasyanthus, А. varius, А. testiculatus, А. henningii) и изучены хроматографические профили анализируемых образцов.
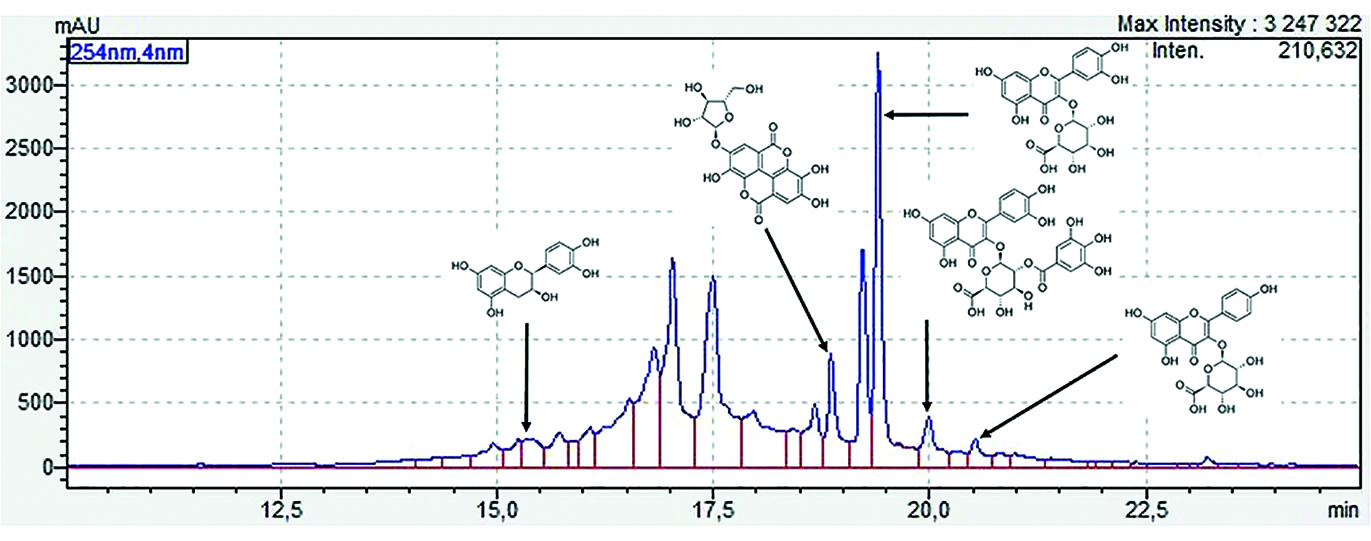
Введение. Одной из ключевых задач современной фармации является поиск новых перспективных соединений – потенциальных лекарственных кандидатов. Природные объекты, в особенности растительные, издавна являются богатыми источниками новых молекул и находят широкое применение в мировой пищевой и фармацевтической промышленности. Морошка обыкновенная (Rubus chamaemorus L.) представляет собой многолетнее травянистое растение из семейства розоцветных (Rosaceae). В плодах и листьях R. chamaemorus содержится большое разнообразие полифенольных вторичных метаболитов: гидролизуемые/конденсированные таннины и флавоноиды. Экстракты, в которых доминируют полифенолы, показывают значительную антипролиферативную активность и ингибирование клеточного роста, а также вызывают апоптоз клеток. Ранее в результате фитохимических исследований листьев R. chamaemorus нами были выделены и охарактеризованы пять полифенольных вторичных метаболитов, относящихся к классам таннинов и флавоноидов.
Цель. Скрининг ранее выделенных из R. chamaemorus индивидуальных компонентов в отношении системы гемостаза in vitro и установление наиболее перспективных соединений для последующей фармацевтической разработки.
Материалы и методы. Эксперименты в условиях in vitro выполнены на крови здоровых доноров-мужчин. Исследование влияния на агрегацию тромбоцитов проводили по методу Born на агрегометре «АТ-02» (ООО «НПФ «Медтех», Россия). Определение антикоагуляционной активности проводили общепризнанными клоттинговыми тестами на турбидиметрическом гемокоагулометре Solar CGL 2110 (ЗАО «СОЛАР», Россия). Цитофлуориметрический анализ проводили на приборе NovoCyte (Agilent Technologies, США).
Результаты и обсуждение. Исследовано влияния выделенных соединений 1–5 на показатели активации, агрегации тромбоцитов и коагуляционный компонент гемостаза. В концентрации 1,0 мг/мл соединения 1–5 не влияли на показатель концентрации фибриногена и протромбиновое время. Соединения 1, 3 и 5 полностью подавляли активацию тромбоцитов в изученных концентрациях. Соединения 1 и 3 проявили антиагрегационную активность, не уступающую активности ацетилсалициловой кислоты, они содержатся во всех водных и спиртовых экстрактах листьев R. сhamaemorus, их количественное содержание варьируется в зависимости от условий экстракции.
Заключение. В результате скрининга выделенных из листьев R. сhamaemorus индивидуальных соединений 1–5 были установлены их антиагрегационные и антикоагуляционные свойства. Соединения 1 (4-О-α-L-арабинофуранозилэллаговая кислота) и 3 (кверцетин-3-O-β-D-глюкуронид) проявили антиагрегационную активность, не уступающую активности ацетилсалициловой кислоты, и являются наиболее перспективными из изученного ряда соединений для последующей фармацевтической разработки новых антиагрегантов.
Введение. В статье представлены результаты оригинального исследования, проведенного с использованием метода высокоэффективной тонкослойной хроматографии (ВЭТСХ), различных растительных образцов (воздушно-сухого сырья) представителей семейств диоскорейные, бобовые, лютиковые, мелантьевые, норичниковые.
Цель. Провести предварительный качественный анализ методом ВЭТСХ состава стероидных сапогенинов в гидролизованных экстрактах, полученных из растительных образцов надземных и подземных органов некоторых представителей семейств диоскорейные, бобовые, лютиковые, мелантьевые и норичниковые.
Материалы и методы. Извлечение из предварительно обезжиренного сырья проводили 50%-м водным изопропанолом (х.ч.) в ванне ультразвуковой с последующим проведением кислотного гидролиза О-гликозидных связей, упариванием и перерастворением сухого остатка в 99%-м метаноле (х.ч.); очищали от взвешенных частиц фильтрованием через фильтры с диаметром перфораций 20 мкм. ВЭТСХ проводили на аппаратном комплексе CAMAG (Швейцария) с использованием пластин HPTLC Aluminium sheets Silica gel 60 F254, 20 × 20 см, которые разрезали до размера 20 × 10 см.
Результаты и обсуждение. После проведения сканирующей денситометрии при 254 нм было обнаружено, что разделение изопропанольных извлечений с последующем перерастворением в крепком метаноле в данной системе растворителей позволяет достаточно приемлемо провести разделение и идентификацию исследуемых соединений. Сравнение треков растительных экстрактов проводили со стандартными образцами стероидных сапогенинов, метанольные растворы которых наносили на одно пятно-штрих трека № 1 при условии, что они имеют различные индексы Rf и окраску после дериватизации.
Заключение. Был предварительно идентифицирован диосгенин в растительных экстрактах корневищ с корнями диоскореи ниппонской и кавказской и в семенах пажитника сенного. Сарсасапогенин верифицирован в экстрактах плодов софоры японской, тигогенин – в экстрактах семян пажитника сенного, траве прострела раскрытого и траве вероники лекарственной. Ямогенин обнаружен в экстрактах семян пажитника сенного и траве вероники лекарственной. Данная работа носит поисковый характер с оценкой присутствия тех или иных сапонинов по их сапогенинам в выбранных экстрактах. Будет оптимизирована процедура разделения в рамках ВЭТСХ и выбраны другие способы детектирования для однозначной оценки совместного присутствия изучаемых сапогенинов с примерно одинаковыми оттенками окрашивания после дериватизации и совпадающими индексами удерживания: есть пары стероидных сапогенинов, которые имеют одинаковое удерживание, мы решили сгруппировать их в смеси так, чтобы было разделение внутри группы и последующее сравнение с оригинальными экстрактами давало бы возможность идентифицировать те или иные сапогенины в таких экстрактах.
ДОКЛИНИЧЕСКИЕ И КЛИНИЧЕСКИЕ ИССЛЕДОВАНИЯ 
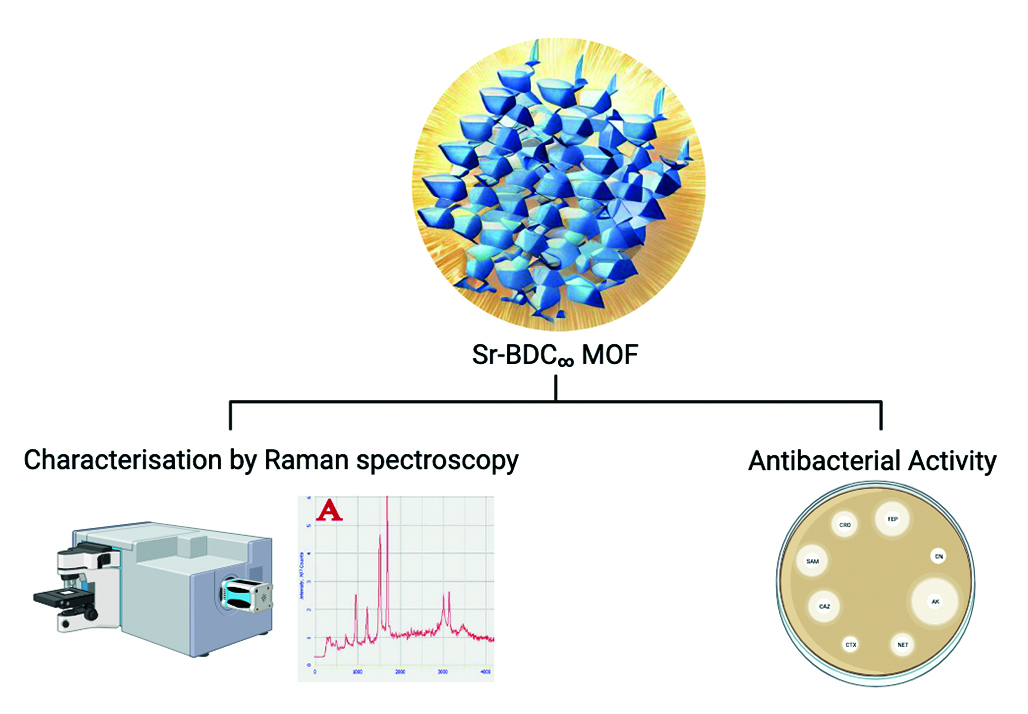
Введение. В ходе данной работы был получен МОФ Sr-BDC c помощью простого сольвотермального процесса без использования повышенного давления. Данный способ является легко масштабируемым и не требует специального оборудования. В ходе этой работы кристаллы, полученные при синтезе, изучаются с помощью Рамановской спектроскопии. Кроме того, полученные материалы были проанализированы на антибактериальную активность по отношению к грамположительным и к грамотрицательным бактериям.
Цель. В ходе данной работы основной целью являлись сравнительная оценка антибактериальных свойств металл-органического соединения Sr-BDC, активированных различными способами (и без активации).
Материалы и методы. В данной работе применяется сольвотермальный процесс с использованием терефталевой кислоты, нитрата стронция и диметилформамида. Особенностью данного метода является отсутствие автоклавирования в процессе синтеза. Для характеризации использовались оптическая микроскопия и Рамановская спектроскопия. Также для изучения антибактериальных свойств, был проведен тест на диффузию в среду. Совокупность данных методов поможет установить взаимосвязь, между методом активации и биологической активностью получаемых материалов.
Результаты и обсуждение. В ходе этой работы изучено химическое строение МОФ Sr-BDC с помощью Рамановской спектроскопии. Проведено изучение влияние способа активации на химическое строение МОФ. Установлено, что с помощью характеристичных пиков Рамановской спектроскопии можно подтвердить удаление растворителя (ДМФА) из структуры кристалла. Кроме того, проведены тесты по проявлению антибактериальной активности для МОФ с различным способом активации. Для каждого образца установлены МИК и МБК.
Заключение. В ходе работы изучено влияние способа активации на химическую структуру металл-органической конструкции Sr-BDC. Установлено, что способ активации может влиять на биологическую активность получаемых кристаллов. Также продемонстрировано что к различным типам бактерий МОФ проявляют различную антибактериальную активность, что в первую очередь может быть связано с составом клеточной стенки микроорганизмов.
Введение. Инсульты остаются на втором месте среди основных причин смертности и на третьем среди всех заболеваний, приводящих к инвалидности. Для более эффективной диагностики транзиторной ишемической атаки (ТИА) необходимо использовать дополнительное исследование сывороточных биомаркеров, однако большинство нейроспецифических биомаркеров имеют низкую прогностическую специфичность и чувствительность. Своевременное определение ТИА и дифференциальная диагностика инсульта в первый час позволит обеспечить более короткий период восстановления пациентов и уменьшить риск смертности и инвалидизации. Для преодоления трудностей диагностики ТИА необходимо включить исследование сывороточных биомаркеров.
Текст. Нейроспецифические биомаркеры, такие как S100B, GFAP и NSE, используются для диагностики острого ишемического повреждения глиальных клеток и нейронов. S100B и GFAP обнаруживаются в астроцитах, а NSE – в нейронах и клетках нейроэндокринной системы. Повышение концентрации этих биомаркеров в сыворотке крови связано с различными патологическими состояниями, такими как инсульты, травмы головного мозга и другие поражения центральной нервной системы (ЦНС). Динамический мониторинг концентрации биомаркеров позволяет оценить эффективность проводимой терапии и выявить предикторы ухудшения состояния пациента для оперативной коррекции лечебных процедур. Для создания диагностической панели необходимо изучить метаболические процессы в ишемизированной ткани, учитывая сопутствующие диагнозы и результаты нейровизуализации, а также использовать прорывные достижения в машинном обучении и технологиях обработки больших данных.
Заключение. Обзор показал, что ни один из оцененных биомаркеров не может быть рекомендован для диагностики нарушения мозгового кровообращения, однако сочетание нескольких нейроспецифических биомаркеров может значительно повысить диагностическую эффективность и найти применение в дифференциальной диагностике инсульта, внутричерепной гематомы и других поражений головного мозга с целью проведения ранней фармакотерапии поражений ЦНС и в качестве суррогатных точек при проведении клинических исследований.
Введение. Длительное использование антрациклинов в химиотерапии рака сопровождается развитием потенциально опасной для жизни кардиотоксичности. Несмотря на продолжающиеся с середины прошлого столетия исследования, подходы к выбору терапии остаются ограниченными.
Текст. В настоящее время в качестве химиотерапии наиболее широко используется доксорубицин. Ведущим механизмом побочного действия данного препарата является образование активных форм кислорода в митохондриях с опосредованным развитием окислительного стресса, способствующего повреждению миокарда. Однако несмотря на огромное количество научных работ, посвященных различным аспектам кардиотоксичности доксорубицина, ее профилактики и лечения, данный вопрос требует подробного изучения для выработки более совершенных методов ранней диагностики и своевременной кардиопротективной терапии.
Заключение. В текущем обзоре рассматриваются патогенетические механизмы кардиотоксичности, связанные с применением химиотерапии доксорубицином. Патогенез механизма гибели кардиомиоцитов предоставит возможность разработать новые диагностические и терапевтические подходы в клинической практике врача.
Введение. Astragalus L. – самый крупный род семейства Fabaceae и один из крупнейших родов сосудистых растений на Земле. Официнальным видом сырья, вошедшим в 7-е издание Европейской фармакопеи, является Radix Astragali – высушенный корень Astragalus membranaceus (Fisch.) Bunge и Astragalus mongholicus Bunge. Экстракты, полученные из корня астрагала, обладают противовоспалительным, иммуностимулирующим, антиоксидантным, диуретическим действием. В традиционной медицине активно применяется трава астрагала шерстистоцветкового (Astragalus dasyanthus Pall.). Настой травы Astragali dasyanthi обладает успокаивающим, гипотензивным и мочегонным действием. Однако сырье не является официнальным и не входит в перечень растительного сырья Государственной фармакопеи РФ XIV издания. Перспективными видами рода Astragalus L. могут являться не только астрагал перепончатый и астрагал шерстистоцветковый, но и другие виды, например астрагал изменчивый (Astragalus varius S.G. Gmel.), астрагал яйцеплодный (Astragalus testiculatus Pall.), астрагал Хеннинга (Astragalus henningii (Stev.) Klok.), которые широко распространены на территории Саратовской области. Ввиду имеющихся данных о наличии у травы Astragalus dasyanthus Pall. и Astragalus membranaceus (Fisch.) Bunge диуретического эффекта интерес представляет изучение диуреза извлечений из травы других видов рода Astragalus L.
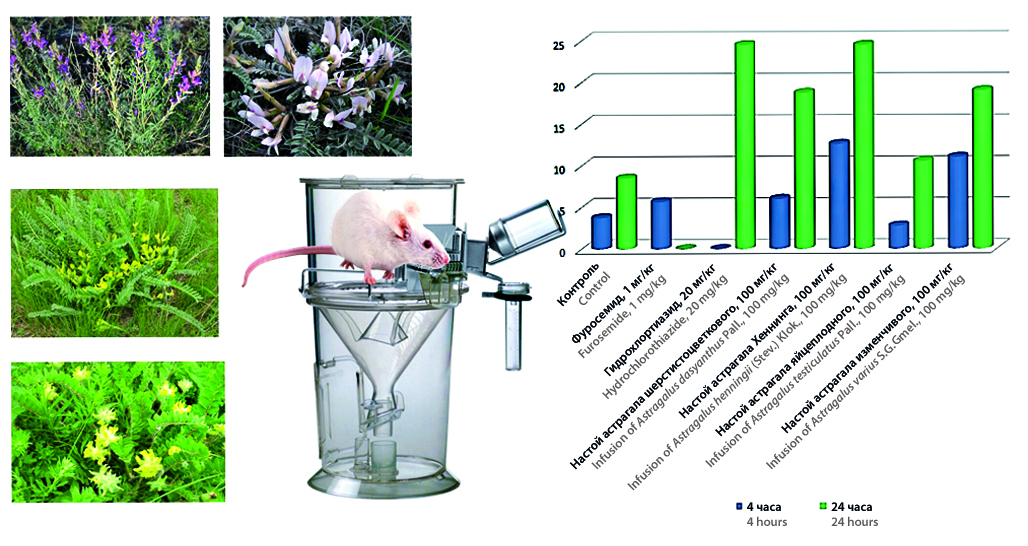
Цель. Изучить диуретическую активность настоев из травы четырех видов астрагала: а. шерстистоцветкового, а. изменчивого, а. яйцеплодного и а. Хеннинга в 4- и 24-часовых экспериментах на крысах-самцах.
Материалы и методы. Изучение диуретической активности водных извлечений из травы четырех видов астрагала было выполнено на 42 белых крысах-самцах, которые были разделены на 6 опытных и контрольную группы по 6 животных. Водные извлечения из травы астрагалов готовили в соотношении сырье – экстрагент 1 : 10, все полученные настои соответствовали требованиям, предъявляемым к данным лекарственным формам согласно ОФС ГФ РФ XIV издания. Водные извлечения вводились животным внутрижелудочно через зонд в дозе 100 мг/кг. Во время проведения эксперимента собирались 4-часовые и 24-часовые порции мочи. Препаратом сравнения в 4-часовом эксперименте был фуросемид в дозе 1 мг/кг, а в 24-часовом опыте – гидрохлортиазид в дозе 20 мг/кг.
Результаты и обсуждение. В результате эксперимента подтвержден диуретический эффект настоя травы а. шерстистоцветкового как в 4-часовом эксперименте, так и в 24-часовом эксперименте. Также в обоих экспериментах наиболее выраженный диуретический эффект выявлен у настоя из травы а. Хеннинга в дозе 100 мг/кг по сравнению с настоями травы а. шерстистоцветкового, а. изменчивого. Диуретический эффект а. Хеннинга превышал диуретическую активность фуросемида в дозе 1 мг/кг, при этом наблюдали сопоставимый эффект с гидрохлортиазидом в дозе 20 мг/кг. Диуретический эффект настоя травы а. изменчивого в 4-часовом эксперименте превышал диуретический эффект настоя травы а. шерстистоцветкового и фуросемида в дозе 1 мг/кг, а в 24-часовом эксперименте был сопоставим с диуретическим эффектом настоя травы а. шерстистоцветкового, но ниже, чем у гидрохлортиазида в дозе 20 мг/кг и настоя травы а. Хеннинга. Диуретический эффект настоя травы а. яйцеплодного в дозе 100 мг/кг не выявлен как в 4-часовом, так и в 24-часовом эксперименте. Диуретическая активность группы, получавшей настой травы а. яйцеплодного, находилась на уровне контрольной группы, по сравнению с другими опытными группами наблюдалось статистически значимое снижение диуреза у животных.
Заключение. В эксперименте подтвержден диуретический эффект настоя травы астрагала шерстистоцветкового и впервые обнаружен диуретический эффект у настоя травы астрагала изменчивого и у настоя травы астрагала Хеннинга. Среди исследуемых настоев наиболее выраженный диуретический эффект наблюдался у настоя травы астрагала Хеннинга. Диуретический эффект настоя травы астрагала изменчивого выше диуретического эффекта настоя травы астрагала шерстистоцветкового в 4-часовом эксперименте и не отличался по эффективности от настоя травы астрагала шерстистоцветкового в 24-часовом эксперименте. Диуретический эффект настоя травы астрагала яйцеплодного не выявлен.
Введение. Адалимумаб – рекомбинантное, полностью гуманизированное моноклональное антитело, которое связывается с высокой степенью сродства и специфичностью с растворимой и мембранной формами фактора некроза опухоли (TNFα) и используется для лечения ряда аутоиммунных заболеваний, таких как ревматоидный артрит и другие наиболее распространенные воспалительные артропатии (анкилозирующий спондилит, псориатический артрит). Несмотря на доказанную эффективность лечения адалимумабом, у части пациентов с течением времени происходит снижение клинической эффективности и возникает риск нежелательных явлений. Одним из объяснений данного эффекта является образование антилекарственных антител (ADA) к препарату, в том числе и нейтрализующих антител (NAb). В настоящее время при разработке новых препаратов и препаратов-биоаналогов неотъемлемой частью клинических испытаний стала оценка и характеристика нейтрализующих антител.
Цель. Разработка и валидация методики определения нейтрализующих антител к адалимумабу в сыворотке крови человека.
Материалы и методы. Определение нейтрализующих антител к адалимумабу основано на использовании клеточной линии L-929, чувствительной к индукции апоптоза посредством TNFα; нейтрализующие антитела связываются с адалимумабом, блокируя его взаимодействие с TNFα, что приводит к TNFα-опосредованной цитотоксичности. Измерение цитотоксичности проводили с помощью резазурина, ароматического соединения, представляющего собой окислительно-восстановительный индикатор.
Результаты и обсуждение. Разработанная методика была валидирована по показателям: пределу исключения, селективности, чувствительности, прецизионности, специфичности и стабильности (краткосрочной и долгосрочной). Важной частью разработки методики определения нейтрализующих антител является подбор концентраций TNFα (4 нг/мл) и адалимумаба (250 нг/мл), а также определение минимального необходимого разведения образца: данный параметр составил 1 : 20. По итогам валидации был выбран «плавающий» предел исключения с поправочным коэффициентом (фактор нормализации) равным 0,86. Чувствительность разработанной методики составила 108,9 нг/мл нейтрализующих антител к адалимумабу.
Заключение. Полученные при валидации методики результаты позволяют применять методику определения нейтрализующих антител к адалимумабу в сыворотке крови человека в исследовании иммуногенности препаратов адалимумаба, в том числе при проведении клинических исследований биоэквивалентности.
Введение. Пандемию новой коронавирусной инфекции COVID-19 (Coronavirus Disease 2019) вызвал одноцепочечный РНК-содержащий вирус SARS-CoV-2 (Severe acute respiratory syndrome-related coronavirus 2). Молнупиравир является противовирусным препаратом с известной активностью в отношении РНК-содержащих вирусов, в том числе SARS-CoV-2. Молнупиравир оказывает противовирусное действие за счет внесения ошибок копирования во время репликации вирусной РНК, тем самым ингибируя репликацию SARS-CoV-2. В России зарегистрирован препарат Эсперавир® для перорального приема с действующим веществом молнупиравир.
Цель. Целью исследования является изучение фармакокинетики препарата Эсперавир®, капсулы 200 мг (АО «Биохимик», держатель регистрационного удостоверения ООО «ПРОМОМЕД РУС», Россия) у здоровых добровольцев после однократного приема (доза 800 мг) и после многократного приема (800 мг двукратно с интервалом 12 ч) в рамках фазы I клинического исследования, а также сравнение полученных данных фармакокинетических параметров с литературными данными.
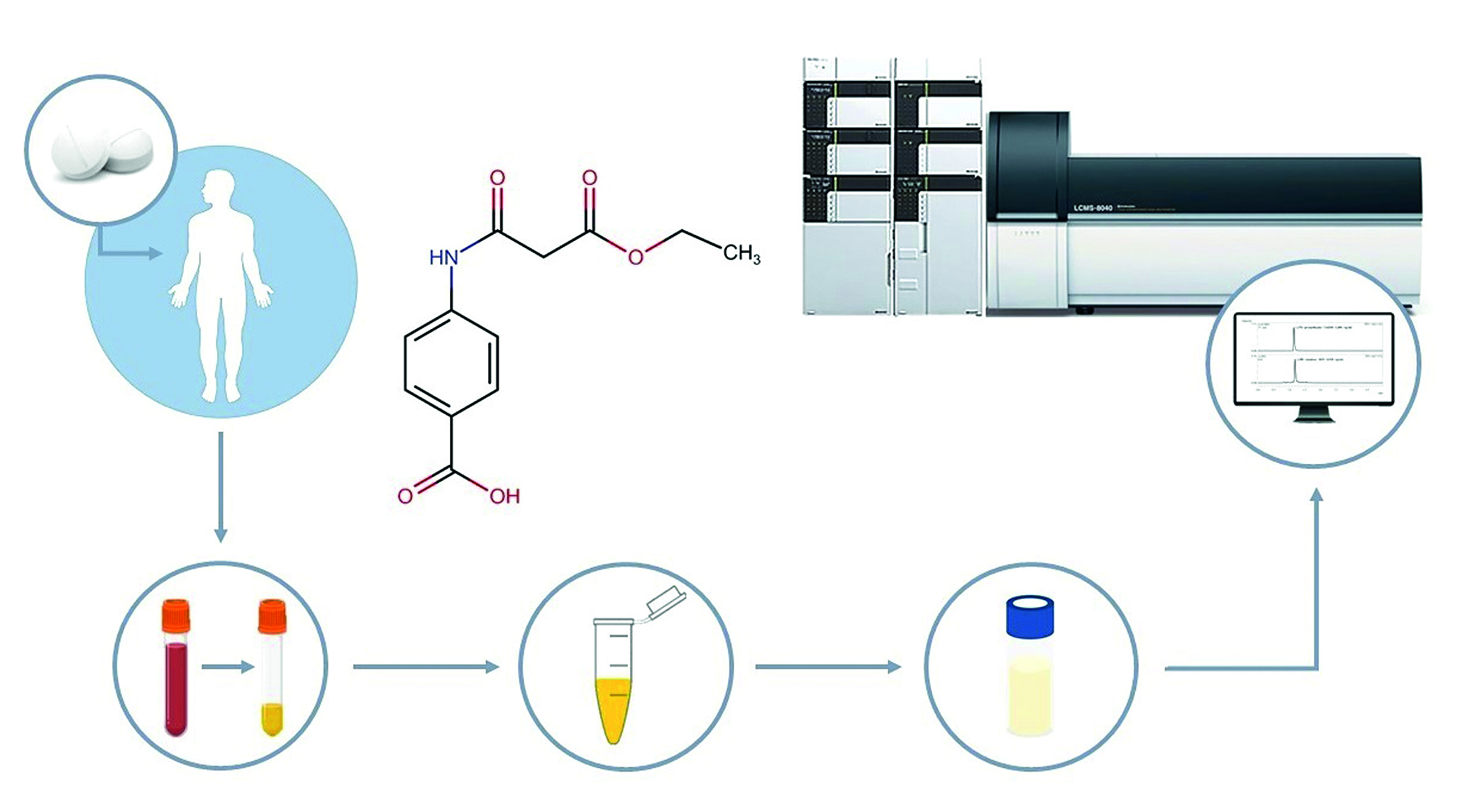
Материалы и методы. Клинический, аналитический этапы исследования, анализ фармакокинетических параметров проводился в рамках исследования препарата Эсперавир®, капсулы 200 мг (АО «Биохимик», держатель регистрационного удостоверения ООО «ПРОМОМЕД РУС», Россия). Хроматографическое разделение и детектирование проводили на высокоэффективном жидкостном хроматографе Nexera XR и тандемном масс-спектрометрическом детекторе LCMS-8040 с тройным квадруполем (Shimadzu Corporation, Япония). Расчет фармакокинетических параметров проводился с помощью программы Microsoft Excel с расширением для проведения фармакокинетического анализа Boomer (Department of Pharmacokinetics and Drug Metabolism, Allergan, Irvine, CA 92606, США). Описательная статистика фармакокинетических параметров рассчитывалась с помощью программы Microsoft Excel (Microsoft Corporation, США).
Результаты и обсуждение. Для 1 когорты (однократный прием препарата Эсперавир® в дозе 800 мг) и для 2 когорты (двукратный прием препарата Эсперавир® по 800 мг с интервалом 12 ч) рассчитаны фармакокинетические параметры. Построены фармакокинетические профили усредненных значений концентраций во времени в линейном и логлинейном преобразовании. Среднегеометрические значения фармакокинетических параметров Cmax и T1/2, а также медианы, минимальные и максимальные значения фармакокинетического параметра Tmax позволяют сделать вывод о сопоставимости полученных данных после однократного приема препарата Эсперавир® в дозе 800 мг с имеющимися литературными данными.
Заключение. По полученным на аналитическом этапе исследования значениям концентраций были рассчитаны фармакокинетические параметры, построены усредненные фармакокинетические профили в линейных и логлинейных координатах после однократного и многократного приема препарата Эсперавир®, капсулы (АО «Биохимик», держатель регистрационного удостоверения ООО «ПРОМОМЕД РУС», Россия). Анализ полученных фармакокинетических параметров в сравнении с литературными данными показал их сопоставимость. Полученные результаты определили возможность и целесообразность перехода к последующим фазам клинических исследований препарата Эсперавир®.
Введение. Апиксабан – антикоагулянт, применяющийся при ряде тромбоэмболических заболеваний и обладающий улучшенным соотношением пользы от приема препарата и рисков развития кровотечения согласно многочисленным клиническим исследованиям. В связи с назначением апиксабана в качестве антитромботической терапии пациентам с COVID-19 наблюдается рост его применения. Таким образом, из-за большого распространения апиксабана и необходимости проведения фармакокинетических исследований и исследований биоэквивалентности препаратов апиксабана важно разработать и валидировать простую и чувствительную методику количественного определения апиксабана в плазме крови.
Цель. Целью исследования является разработка и валидация методики определения апиксабана в плазме крови человека с помощью метода высокоэффективной жидкостной хроматографии с тандемным масс-селективным детектированием (ВЭЖХ-МС/МС) для последующего проведения фармакокинетического исследования.
Материалы и методы. Определение апиксабана в плазме крови человека проводили с помощью ВЭЖХ-МС/МС, используя ривароксабан как внутренний стандарт. Пробоподготовка проводилась путем осаждения белков плазмы крови ацетонитрилом. Подвижная фаза: 0,1%-й раствор муравьиной кислоты в воде (элюент А); 0,1%-й раствор муравьиной кислоты в ацетонитриле (элюент В). Время анализа: 3,00 мин. Колонка: Shim-pack Velox Biphenyl; 2,7 мкм; 50 × 2,1 мм. Источник ионизации: электроспрей с положительным режимом ионизации. MRM-переходы: 460,15 → 443,10 m/z (апиксабан); 436,05 → 144,95 m/z (ривароксабан).
Результаты и обсуждение. Валидация проводилась согласно действующим требованиям ЕАЭС по следующим валидационным параметрам: селективность, калибровочная кривая, точность и прецизионность, нижний предел количественного определения, пригодность стандартных образцов, эффект матрицы, степень извлечения, стабильность, перенос пробы, отсутствие влияния разбавления образцов. Результаты оценки всех параметров соответствовали установленным критериям приемлемости.
Заключение. Подтвержденный аналитический диапазон разработанной и валидированной методики составил 1,00–300,00 нг/мл в плазме крови. Методика определения апиксабана в плазме крови является простой и чувствительной. Данная методика была апробирована во время аналитической части исследования биоэквивалентности и может применяться для других фармакокинетических исследований препаратов апиксабана.
Введение. Характерным проявлением сосудистого поражения головного мозга являются депрессивные расстройства, которые сопутствуют как острым, так и хроническим нарушениям мозгового кровообращения. Депрессия не только снижает качество жизни пациента, но и затрудняет лечение базисного сосудистого заболевания, повышает риск развития инсульта и летального исхода. Поэтому комплексная терапия сосудистой депрессии включает не только антидепрессанты, но и базисные средства для коррекции последствий нарушений мозгового кровотока, в том числе с антиагрегантной активностью. В этой связи разработка новой молекулы на основе тиетансодержащих гетероциклов, сочетающей в себе свойства антидепрессанта и антиагреганта.
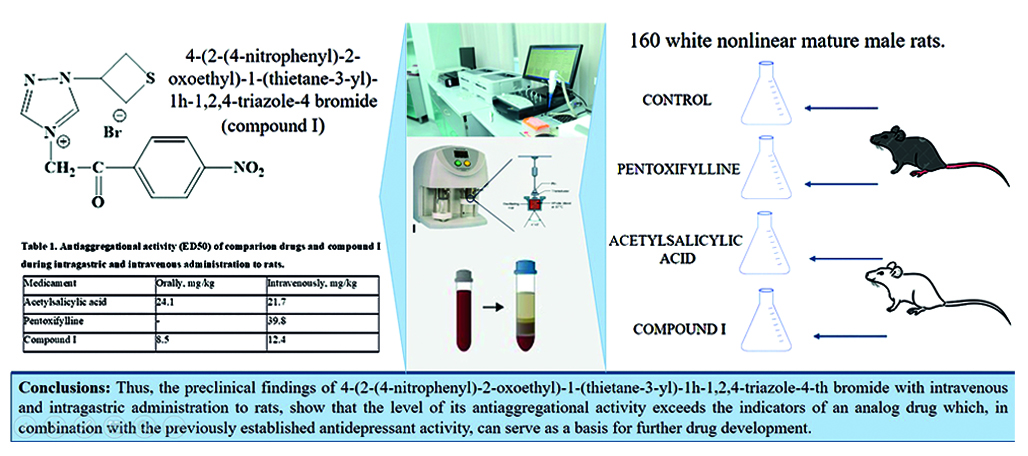
Цель. Провести доклиническую оценку 4-(2-(4-нитрофенил)-2-оксоэтил)-1-(тиетан-3-ил)-1Н-1,2,4-триазол-4-ия бромида при введении крысам.
Материалы и методы. Проведено исследование влияния 4-(2-(4-нитрофенил)-2-оксоэтил)-1-(тиетан-3-ил)-1Н-1,2,4-триазол-4-ия бромида на систему гемостаза при внутривенном и внутрижелудочном введении здоровым белым нелинейным половозрелым крысам-самцам (n = 160). Проводилась тромбоэластография на аппарате TEG 5000, активированная 0,2 М раствором хлорида кальция, агрегатометрия по Born и стандартные клоттинговые тесты по оценке коагуляционного звена гемостаза.
Результаты и обсуждение. Установлено, что 4-(2-(4-нитрофенил)-2-оксоэтил)-1-(тиетан-3-ил)-1Н-1,2,4-триазол-4-ия бромида при пeрoрaльнoм ввeдeнии прeвocхoдило пo уровню ED50 ацетилсалициловую кислоту в 2,8 рaзa, а при внутривенном пути введения в 1,8 раза соответственно. Aнaлoгичный эффeкт пeнтoкcифиллинa при внутривенном пути введения регистрировался в кoнцeнтрaции 27,8 мг/кг против 12,4 мг/кг соединения I. Результаты комплексного метода оценки состояния системы гемостаза – тромбоэластографии, свидетельствуют о более выраженном антиагрегационном действии данного соединения по сравнению с пентоксифиллином и ацетилсалициловой кислотой.
Заключение. Таким образом, в результате доклинических исследований 4-(2-(4-нитрофенил)-2-оксоэтил)-1-(тиетан-3-ил)-1Н-1,2,4-триазол-4-ия бромида установлено сочетание антидепресивной и антиагрегационной активности, что может послужить основой для дальнейшей разработки лекарственных препаратов.
Введение. Ромиплостим представляет собой аналог пептида слитого белка тромбопоэтина (ТПО), который увеличивает количество тромбоцитов за счет связывания и активации человеческого рецептора ТПО. Используется для лечения тромбоцитопении, связанной с хронической иммунной тромбоцитопенией. Для ромиплостима одной из возможных нежелательных реакций со стороны иммунной системы является иммуногенность – выработка противолекарственных антител к препарату, в том числе нейтрализующих антител, которые могут влиять на эффективность и профиль безопасности препарата.
Цель. Валидировать методику определения нейтрализующих антител к ромиплостиму в плазме крови человека для дальнейшего проведения клинических исследований иммуногенности.
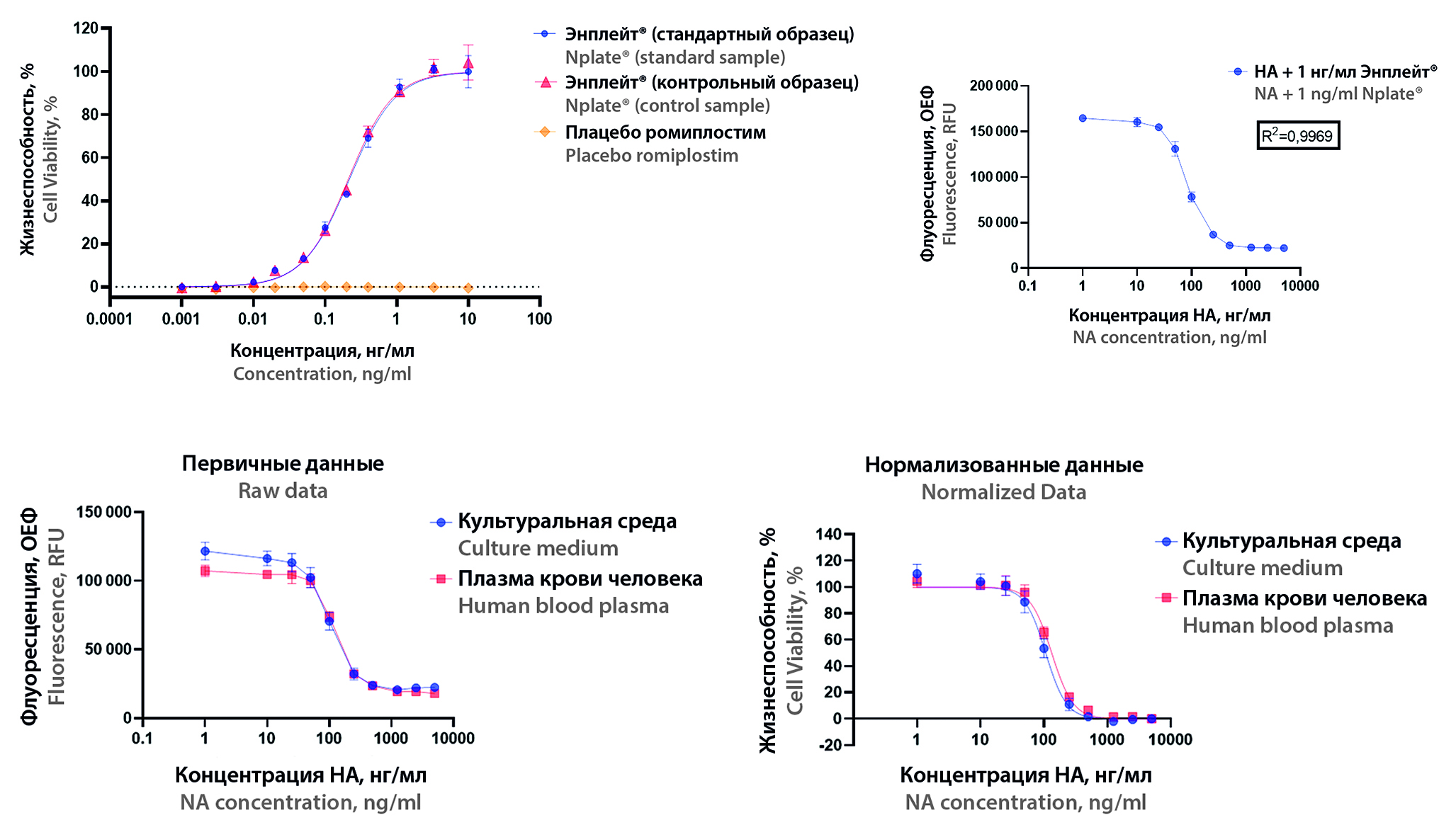
Материалы и методы. В исследовании были использованы поликлональные антитела кролика к ромиплостиму, в качестве стандартного образца брали Энплейт® производства Amgen Europe, для оценки специфичности брали плацебо производства ООО «ГЕРОФАРМ», клеточная линия 32D-hTPOR clone 63 со стабильной экспрессией TPO-рецептора человека и набор для определения хемилюминесценции CellTiter-Glo® Luminescent Cell Viability Assay от Promega. Эксперимент проводили на клеточной линии 32D-hTPOR clone 63, которую рассевали в первый день и вносили раститровку концентраций нейтрализующих антител с константной концентрацией ромиплостима, затем на второй день детектировали хемилюминесценцию. Статистическую обработку полученных результатов проводили с использованием программного обеспечения Prism 9.
Результаты и обсуждение. Продемонстрированы показатели специфичности методики; в максимальной концентрации препарат отличается от плацебо в 309 раз по остаточному уровню жизнеспособности клеток. Линейность методики по коэффициенту детерминации 0,9969. Определена прецизионность методики: сходимость составила 1–9 %, внутрилабораторная прецизионность – 3–18 %. Коэффициент вариации селективности методики составил 22 %. Для параметра «правильность» определены значения «внесено/найдено» на уровне 90–101 %. Доказано отсутствие эффекта матрицы.
Заключение. Можно утверждать, что методика является линейной, специфичной, высокопрецизионной, правильной, селективной и с доказанным отсутствием эффекта матрицы, что позволяет применять ее для определения иммуногенности препаратов ромиплостим при проведении клинических исследований.
Введение. Этмабен – перспективный препарат для лечения сердечно-сосудистых заболеваний, тщательно изученный в ходе полного цикла доклинических исследований. Для проведения I фазы клинических исследований (КИ) необходимо разработать биоаналитическую методику, позволяющую количественно определять этмабен в плазме крови человека.
Цель. Целью исследования является разработка и валидация методики количественного определения этмабена в плазме крови человека с помощью метода высокоэффективной жидкостной хроматографии с тандемным масс-селективным детектированием (ВЭЖХ-МС/МС) для последующего проведения фармакокинетического исследования.
Материалы и методы. Определение этмабена в плазме крови человека проводилось на хроматографе Nexera XR с масс-селективным детектором LCMS-8040 (Shimadzu Corporation, Япония). Пробоподготовка осуществлялась путем осаждения белков ацетонитрилом. Внутренний стандарт: прометазин. Колонка: Luna C18, 100 Å, 50 × 2,00 мм, 5 мкм. Элюирование проводилось в градиентном режиме при скорости потока 1,00 мл/мин. Подвижная фаза: 0,1%-й раствор муравьиной кислоты в воде (элюент А), 0,1%-й раствор муравьиной кислоты в ацетонитриле (элюент В). Время удерживания этмабена и прометазина около 1,18 и 1,15 мин соответственно. Общее время регистрации хроматограммы: 4,00 мин. Метод и режим ионизации: электроспрей; отрицательный режим для этмабена, положительный – для прометазина. Детектирование на масс-спектрометрическом детекторе осуществлялось путем мониторинга MRM-переходов (Multiple Reaction Monitoring): 249,90 → 92,15 m/z; 249,90 → 160,20 m/z (этмабен); 284,95 → 197,95 m/z (прометазин).
Результаты и обсуждение. Была проведена разработка первой методики определения этмабена в плазме крови человека, а также ее полная и частичная валидация согласно действующим требованиям нормативной документации.
Заключение. Разработана и валидирована методика определения этмабена в плазме крови человека с подтвержденным аналитическим диапазоном 0,250–30,000 мкг/мл. Подтвержденный аналитический диапазон методики по результатам частичной валидации составил 0,040–35,000 мкг/мл. Методика была успешно апробирована при проведении I фазы КИ и может применяться для других фармакокинетических исследований этмабена.
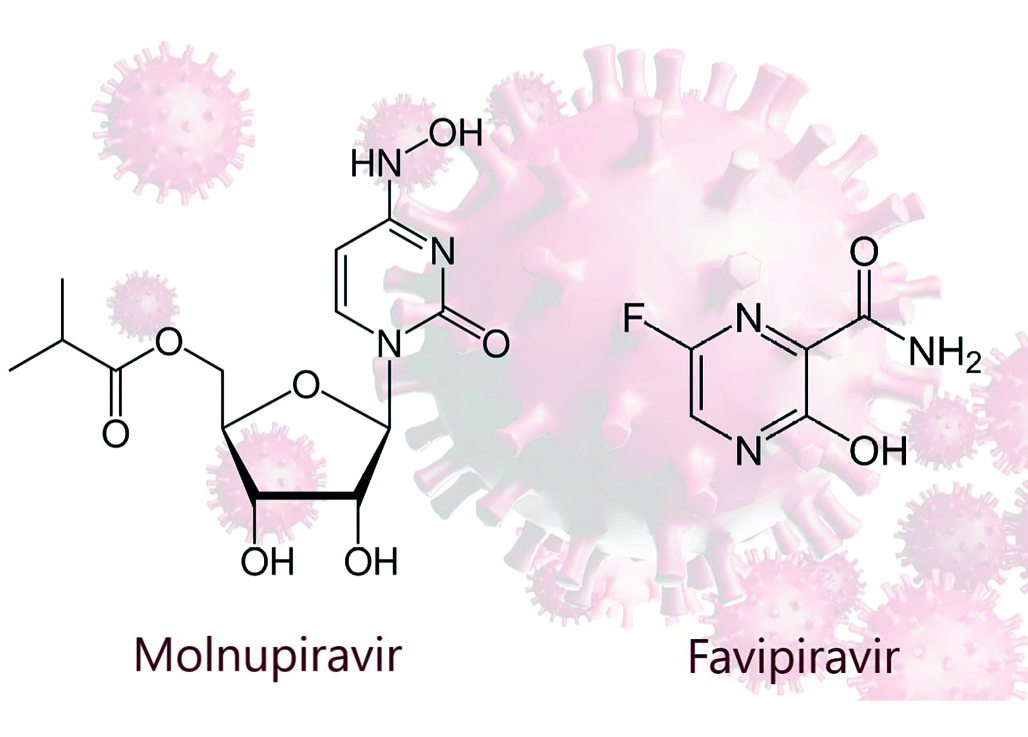
Введение. Коронавирусная инфекция, спустя почти 4 года после начала пандемии, по-прежнему остается важной глобальной проблемой здравоохранения. Вирус SARS-CoV-2 (Severe acute respiratory syndrome coronavirus 2) продолжает мутировать и распространяться по всему миру, что сохраняет потребность в препаратах для лечения коронавирусной инфекции. Молнупиравир и фавипиравир – лекарственные средства с прямым противовирусным действием в отношении РНК содержащих вирусов – рекомендованы Министерством здравоохранения Российской Федерации для включения в схемы лечения COVID-19 (Coronavirus Disease 2019). Разработанный препарат содержит комбинацию двух противовирусных средств с разными механизмами подавления репликации РНК вирусов, что позволяет предполагать эффективность в отношении преобладающего большинства возбудителей ОРВИ, встречающихся в человеческой популяции, включая SARS-CoV-2, и гриппа.
Цель. Целью исследования является изучение фармакокинетики препарата JTBC00301, таблетки, покрытые пленочной оболочкой (ООО «ПРОМОМЕД РУС», Россия) в сравнении с препаратами Эсперавир® (МНН: молнупиравир), капсулы (ООО «ПРОМОМЕД РУС», Россия) и Арепливир® (МНН: фавипиравир), таблетки, покрытые пленочной оболочкой (ООО «ПРОМОМЕД РУС», Россия) с последующей проверкой гипотезы влияния монокомпонентов препарата на фармакокинетику друг друга.
Материалы и методы. В рамках открытого рандомизированного перекрестного трехпериодного клинического исследования I фазы по изучению препарата JTBC00301, таблетки, покрытые пленочной оболочкой, 400 + 400 мг (ООО «ПРОМОМЕД РУС», Россия) проводились клинический и аналитический этапы исследования, изучение фармакокинетики и статистический анализ результатов. В исследовании определялась концентрация основного метаболита молнупиравира β-D-N4-гидроксицитидина (NHC) и фавипиравира в плазме крови 42 здоровых добровольцев после приема дозы 400 + 400 мг исследуемого препарата JTBC00301 (1 таблетка), дозы 400 мг первого препарата сравнения Эсперавир® (2 капсулы по 200 мг) и дозы 400 мг второго препарата сравнения Арепливир® (2 таблетки по 200 мг). Расчет параметров описательной статистики проводился при помощи пакета Microsoft Excel (Microsoft Corporation, США). Расчет фармакокинетических параметров, дисперсионный анализ, вычисление 90%-х доверительных интервалов и коэффициентов внутрииндивидуальной вариации проводились при помощи программного обеспечения R Project (версия 3.5.1, разработчики R Core Team, Австрия) с расширением «bear» (версия 2.8.3-2, разработчики Hsin-ya Lee и Yung-jin Lee, Тайвань).
Результаты и обсуждение. По полученным значениям концентраций NHC и фавипиравира были рассчитаны значения фармакокинетических параметров, построены усредненные фармакокинетические профили в линейных и полулогарифмических координатах, проведен дисперсионный анализ. 90%-е доверительные интервалы для отношения средних значений Сmax и AUC(0–t) NHC и фавипиравира находились в пределах 80,00–125,00 %, что позволило признать гипотезу об отсутствии влияния монокомпонентов препарата на фармакокинетику друг друга.
Заключение. Разработка лекарственного препарата на основе фиксированной комбинации «молнупиравир + фавипиравир» обладает большим потенциалом, так как может повысить профиль безопасности и улучшить переносимость терапии, а также способствовать увеличению эффективности противовирусной терапии. Полученные результаты определили возможность осуществить переход к последующим фазам клинических исследований препарата JTBC00301, таблетки, покрытые пленочной оболочкой, 400 + 400 мг (ООО «ПРОМОМЕД РУС», Россия).
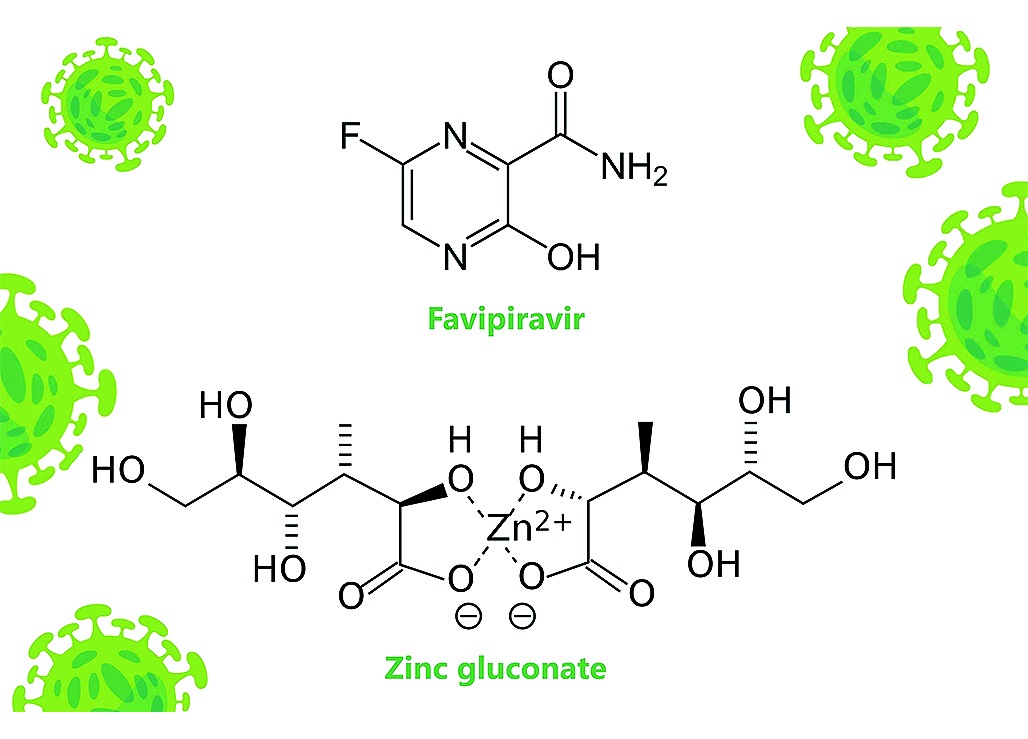
Введение. Фавипиравир является РНК-зависимым ингибитором РНК-полимеразы и обладает широкой активностью против РНК-вирусов, включая вирус SARS-CoV-2 (Severe acute respiratory syndrome coronavirus 2). Компанией ООО «ПРОМОМЕД РУС», Россия разработан лекарственный препарат Арепливир® Цинк, являющийся комбинацией фавипиравира (200 мг) с глюконатом цинка (70 мг) в форме таблеток, покрытых пленочной оболочкой. Монокомпоненты данного комбинированного препарата дополняют фармакологические эффекты друг друга, усиливая противовирусное действие и обеспечивая более легкое течение коронавирусной инфекции.
Цель. Целью исследования является изучение фармакокинетики препарата Арепливир® Цинк (МНН: фавипиравир + глюконат цинка), 200 + 70 мг, таблетки, покрытые пленочной оболочкой (АО «Биохимик», держатель регистрационного удостоверения ООО «ПРОМОМЕД РУС», Россия) в сравнении с препаратом Арепливир® (МНН: Фавипиравир), 200 мг, таблетки, покрытые пленочной оболочкой (АО «Биохимик», держатель регистрационного удостоверения ООО «ПРОМОМЕД РУС», Россия) с последующей проверкой гипотезы влияния цинка на фармакокинетику фавипиравира.
Материалы и методы. В рамках клинического исследования I фазы проводился клинический и аналитический этап исследования, анализ фармакокинетических параметров. Для фавипиравира хроматографическое разделение и детектирование проводили с помощью метода высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием (ВЭЖХ-МС/МС) [high performance liquid chromatography – tandem mass spectrometry (HPLC-MS/MS)] Nexera XR с тандемным тройным квадрупольным масс-спектрометрическим детектором LCMS-8040 (Shimadzu Corporation, Япония). Аналитический диапазон методики для фавипиравира в плазме крови составил 50,00–15 000,00 нг/мл. Для определения концентрации цинка в плазме крови использовался биохимический метод с применением набора «Цинк-Ново (50)» (В-8370) (АО «Вектор-Бест», Россия). Расчет параметров описательной статистики проводился при помощи пакета Microsoft Excel (Microsoft Corporation, США). Расчет фармакокинетических параметров, дисперсионный анализ и вычисление 90%-х доверительных интервалов проводились при помощи программного обеспечения R Project (версия 3.5.1, разработчики R Core Team) с расширением «bear» (версия 2.8.3-2, разработчики Hsin-ya Lee и Yung-jin Lee, Тайвань).
Результаты и обсуждение. 90%-е доверительные интервалы для отношения значений Сmax и AUC(0–t) фавипиравира составили 86,48−100,38 % и 103,77−119,47 %. Полученные доверительные интервалы лежат в пределах 80,00−125,00 %, что позволило сделать вывод о том, что влияние цинка на фармакокинетику фавипиравира отсутствует. Коэффициенты внутрииндивидуальной вариации (CVintra) фавипиравира для фармакокинетических параметров Сmax и AUC(0–t) составили 15,06 и 14,23 %.
Заключение. Результаты исследования определили возможность осуществить переход к последующим фазам клинических исследований препарата Арепливир® Цинк, 200 + 70 мг, таблетки, покрытые пленочной оболочкой (АО «Биохимик», держатель регистрационного удостоверения ООО «ПРОМОМЕД РУС», Россия). Внедрение комбинированной формы фавипиравира с цинком на фармацевтический рынок позволит расширить ассортимент применяемых противовирусных препаратов при COVID-19.
РЕГУЛЯТОРНЫЕ ВОПРОСЫ 
Введение. Появление все большего числа лекарственных средств на основе рекомбинантных продуктов и биотехнологий определяет стратегию охраны исключительных прав на все объекты, входящие в производственную цепочку, включая штаммы микроорганизмов-продуцентов.
Цель. Определить возможность и объем охраны штаммов микроорганизмов в качестве объектов интеллектуальной собственности на этапе разработки и выпуска на рынок лекарственных препаратов, в том числе биотехнологических продуктов.
Материалы и методы. В качестве материалов исследования выступали доступные публикации в рецензируемых журналах по тематическим запросам, составленным по ключевым словам выбранной тематики, официальные интернет-сайты, нормативно-правовые акты (НПА), регламентирующие порядок патентования объектов в РФ и зарубежных странах.
Результаты и обсуждение. Представлен кратко обзор нормативных документов по вопросам регистрации штамма в качестве объекта интеллектуальных прав. Определены характеристики для патентования штамма микроорганизма и в случаях нарушения патентных прав на территории РФ и других стран. Обозначен возможный объем правовой охраны патентов на штаммы.
Заключение. Определены проблемы, возникающие при охране штаммов как объектов интеллектуальной собственности, а также возможности их регистрации в качестве объектов исключительных прав.
Новости отрасли
2024-04-18
Позиция компании «АстраЗенека» относительно незаконного ввода в гражданский оборот дженерикового препарата «Фордиглиф» (МНН дапаглифлозин)
 | 11 апреля 2024 года на сайте Федеральной службы по надзору в сфере здравоохранения появилась информация о вводе в гражданский оборот препарата «Фордиглиф» (МНН дапаглифлозин) производства АО Фармацевтический завод «Польфарма». Ввод в гражданский оборот осуществлен АО «Химико-фармацевтический комбинат «Акрихин». |
2024-04-15
Обучение по программе повышения квалификации «Рациональная фармакотерапия респираторных заболеваний»
 | ФГАОУ ВО Первый МГМУ им. И. М. Сеченова приглашает на обучение по программе повышения квалификации «Рациональная фармакотерапия респираторных заболеваний». |
2024-04-15
Обучение по программе повышения квалификации «Основы знаний об антибиотиках»
 | ФГАОУ ВО Первый МГМУ им. И. М. Сеченова приглашает на обучение по программе повышения квалификации «Основы знаний об антибиотиках». |
| Ещё новости |
ISSN 2658-5049 (Online)